Determinación de valores de referencia para la microtécnica de fagocitosis y muerte intracelular deCándida álbicans en un grupo de población sana en Bogotá
Jeannette Navarrete O M.Sc.1, Gladys Pinilla B M.Sc1., Liliana Muñoz M.Sc1., Ariel I. Ruiz Parra MD2, Yolanda Cifuentes MD2
1Universidad Colegio Mayor de Cundinamarca Facultad de Ciencias de la Salud Programa de Bacteriología y Laboratorio Clínico
1Universidad Nacional de Colombia
Correspondencia: jnavarreteo@unicolmayor.edu.co
Recibido: 04-06-2007 / Aceptado: 28-06-2007
Los macrófagos participan en etapas más tardías de la inflamación fagocitando bacterias y restos celulares. Las técnicas de evaluación de la capacidad fagocítica han mostrado ser muy laboriosas, requieren gran cantidad de muestra sanguínea y excesiva manipulación de las células analizadas. Por el contrario, la microtécnica de muerte intracelular de Cándida para el análisis de la función fagocítica es una técnica rápida, poco dispendiosa y que requiere de muy poca cantidad de sangre. En este trabajo se analizaron 56 muestras de personas sanas con la microtécnica de muerte intracelular de Candida albicans, para hallar valores normales del índice de fagocitosis y el porcentaje de muerte intracelular, indicadores que evalúan la capacidad fagocítica de los polimorfonucleares neutrófilos.
El índice de fagocitosis fue de 2.70 +/- 0.43 (media +/- DE) con un rango de 2.03 a 3.92 y el porcentaje de muerte Intracelular fue de 31.31 +/- 5.10 (media +/- DE) con un rango de 21 a 39. No hubo diferencias por grupos de edad, género, recuento de leucocitos o porcentaje de polimorfonucleares.
Palabras clave: Cándida albicans, fagocitosis, inmunidad innata, opsonin, polimorfonuclear neutrófilo.
Macrophages participate in late stages of inflammation phagocyting bacteria and cellular debris. The techniques for evaluation of the phagocytic capacity are laborious, require large blood samples and need excessive manipulation of the cells. The micro technique of intracellular death of Candida albicans is a simple and fast technique, which requires a very little blood sample. This technique was used in 56 samples of healthy people to determine reference values of the phagocytic index and the percentage of intracellular death, which are indicators of neutrophils´ phagocytic capacity.
The phagocitic index was 2.70 +/- 0.43 (mean +/- SD), range 2.03 - 3.92, and the percentage of intracellular death was 31.31 +/- 5.10 (mean +/- SD), range 21 - 39. There were no differences by age groups, gender and number of leucocytes or percentage of neutrophils.
Key words: Cándida albicans, innate immunity, neutrophils, opsoninas, phagocytosis.
La fagocitosis es un mecanismo básico de defensa presente en la mayoría de las especies. En los mamíferos está a cargo de células especializadas, principalmente los polimorfonucleares neutrófilos (PMN) y los macrófagos. Los primeros son células sanguíneas circulantes que se ponen en contacto con el material a fagocitar a través de la respuesta inflamatoria. Los macrófagos provienen de monocitos circulantes o bien están distribuidos estratégicamente en los tejidos. Ambos presentan diferencias en su poder fagocítico (2,3).
La fagocitosis es el proceso por el cual las células especializadas buscan, localizan, identifican e introducen a su citoplasma partículas o gérmenes extraños. Los fagocitos poseen receptores para el componente C3b del sistema de complemento, así como para la región constante de la molécula de inmunoglobulina, lo que permite que los microorganismos opsonizados puedan adherirse a la superficie de estas células, facilitando la fagocitosis (4).
Los PMN son especialmente efectivos durante el inicio de infecciones por bacterias extracelulares Gram positivas y Gram negativas, ya que estas bacterias tiene una superficie hidrofóbica y poco cargada eléctricamente por lo que son reconocidas y fagocitadas sin dificultad. Los macrófagos participan en etapas más tardías de la inflamación fagocitando bacterias y restos celulares. Estas células son importantes en la defensa ante bacterias intracelulares y generalmente actúan concomitantemente con respuestas inmunes adaptativas (4,5).
Existen pruebas de laboratorio para evaluar el sistema inmune; sin embargo, algunas de éstas son dispendiosas, requieren de tiempo y gran cantidad de muestra sanguínea lo que podría causar una alteración en la evaluación funcional del sistema inmune (6). Este trabajo tiene por objetivos describir el micro método para evaluar la capacidad fagocítica y de muerte intracelular de cándida realizada por los PMN descrito por Oseas (7) y determinar valores de referencia en una población sana en Bogotá.
Sujetos de estudio
Se obtuvieron muestras sanguíneas de 100 sujetos voluntarios asintomáticos con edades comprendidas entre los 15 y los 51 años de edad, durante el periodo del 16 de abril al 22 de mayo de 2007. Los criterios de inclusión para considerar como sanos a los sujetos de estudio fueron: índice de masa corporal (IMC) entre 18 y 25 Kg/m2, recuento de leucocitos entre 5.000/fL y 10.000/fL, hemoglobina en hombres entre 13 g/dL y 17 g/dL y en mujeres entre 12 g/dL y 16 g/dL; hematocrito entre 40% y 48% en hombres y entre 36% y 44% en mujeres y el porcentaje de neutrófilos entre 45% y 70% (8). Cincuenta y seis muestras cumplieron los criterios de inclusión.
Muestra
Se tomaron 4 mL de sangre periférica para la realización del cuadro hemático y 3 gotas de sangre sin anticoagulante evitando el contacto con el vidrio para la microtécnica de fagocitosis y muerte intracelular de Cándida. El cuadro hemático se realizó utilizando el sistema CELL-DYN 1400 siguiendo las indicaciones del fabricante (Abbott Diagnostics, U.S.A).
Obtención de células adherentes (polimorfonucleares neutrófilos)
Tres gotas de sangre sin anticoagulante se colocaron en una laminilla de vidrio de 22 x 22mm, con reborde definido de 1cm de diámetro; estas muestras fueron incubadas en cámara húmeda a 37°C por 1 hora. El coagulo se retiró y la laminilla fue lavada con solución buffer de Hank´s (pH 7.2) precalentada a 37C, para retirar las células no adherentes. Cada muestra fue procesada por duplicado.
Solución de Cándida albicans
De un cultivo no mayor de 24 horas de Cándida albicans en agar Saboreaud se tomó una alícuota, lacual fue lavada tres veces con solución de Hank´s precalentada a 37°C, para obtener una concentración final de 2 x 106 UFC/mL de cándida.
Pool de opsoninas
Como fuente de opsoninas (complemento e inmunoglobulinas) se usó un pool de sueros de personas normales que fue separado en alicuotas y conservado a -80°C hasta el momento de su uso.
Microtécnica de fagocitosis y muerte intracelular de Cándida albicas
Las células adheridas al vidrio fueron incubadas a 37°C durante 10 minutos en cámara húmeda con 120 _L de la solución de Cándida albicans y 50 _L del pool de opsoninas. Posteriormente, las laminillas fueron lavadas 2 veces con solución de buffer Hank´s, previamente precalentada a 37°C; adicionalmente, para evitar la desecación, se adicionaron 200 _L del buffer a las células adheridas e incubadas en cámara húmeda a 37°C durante 40 minutos. Finalmente, la tinción de células vivas y muertas se llevó a cabo adicionando 50 _L de solución de azul de metileno (1M en solución de Hank´s) e incubado por 10 minutos a 37°C en cámara húmeda.
La lectura se realizó en microscopio de luz, contando 100 PMN con el número total de cándidas fagocitadas. El índice de fagocitosis se calcula teniendo en cuenta el número de cándidas que fagocitó un PMN. Para la muerte intracelular de cándida, el porcentaje es calculado teniendo en cuenta del total de cándidas fagocitadas, cuantas captaron el colorante (cándidas muertas).
Análisis estadístico
Las variables categóricas se describen como porcentajes. La distribución de las variables continuas se analizó usando la prueba de Shapiro-Wilk. Los datos se presentan como medias y desviaciones estándar o medianas y percentiles según sea apropiado de acuerdo con su distribución. Se aplicó la prueba de t-student para comparación de medias y se obtuvieron gráficas de dispersión e índices de correlación de variables continuas. El análisis estadístico se realizó usando el programa STATA 8.0.
Aspectos éticos
El protocolo fue aprobado por el comité de ética de la Universidad Colegio Mayor de Cundinamarca y todos los sujetos aceptaron y firmaron el consentimiento informado.
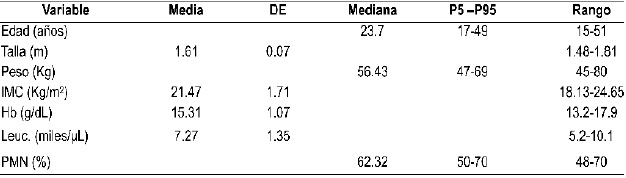
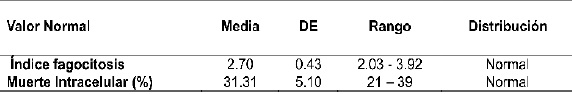
Tabla 1. Variables antropométricas y de laboratorio de los 56 sujetos voluntarios sanos.

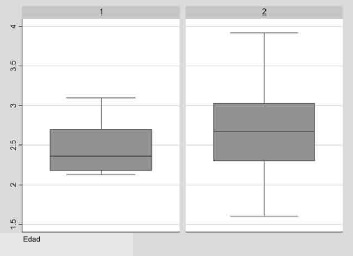
Figura 1. Distribución del índice de fagocitosis en sujetos sanos menores (1) y mayores de 18 años (2).
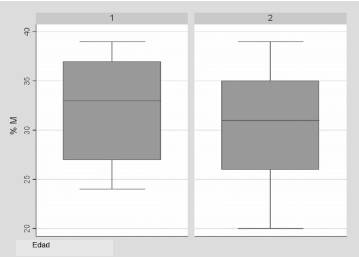
Figura 2. Distribución del porcentaje de muerte intracelular de Cándida en sujetos sanos menores (1) y mayores de 18 años (2).
El 78.51% de las muestras provenían de mujeres. No se encontraron diferencias estadísticamente significativas en la función fagocítica de los PMN entre hombres y mujeres (p = 0.35). Figuras 3 y 4.
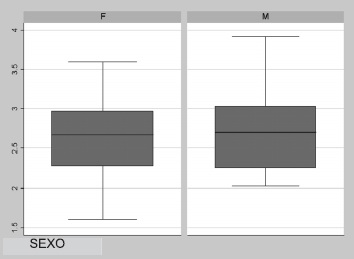
Figura 3. Distribución del índice de fagocitosis en mujeres (F) y hombres (M) voluntarios sanos usando la microtécnica de fagocitosis y muerte intracelular de Cándida albicans.
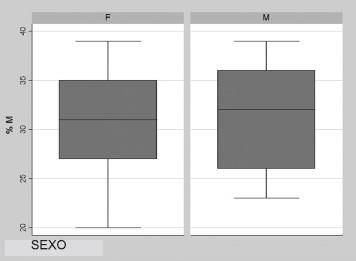
Figura 4. Distribución del porcentaje de muerte intracelular en mujeres (F) y hombres (M) voluntarios sanos usando la microtécnica de fagocitosis y muerte intracelular de Cándida albicans.
No se encontró una correlación estadísticamente significativa entre el recuento de leucocitos y el índice de fagocitosis (r = -0.04, p = 0.76, Figura 5A), ni el porcentaje de muerte celular (r = - 0.15, p = 0.25, Figura 5B).
Tabla 2. Valores de referencia para el índice de fagocitosis y muerte intracelular de Cándida en población adulta
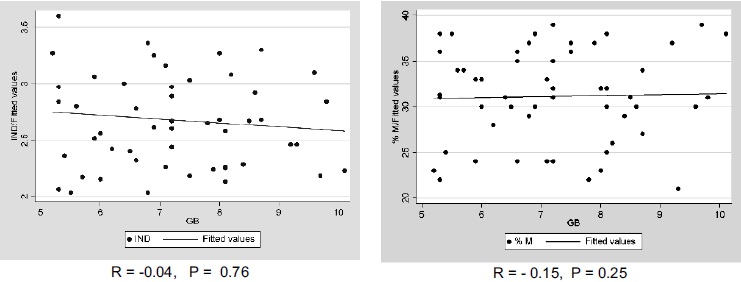
Figuras 5. Correlación entre número de leucocitos y el índice de fagocitosis (A) y el porcentaje de muerte intracelular de Cándida (B). GB: glóbulos blancos.
Tampoco se encontró una correlación estadísticamente significativa entre el porcentaje de neutrófilos PMN y el índice de fagocitosis (r = 0.13, p = 0.30, Figura 6A) o el porcentaje de muerte intracelular (r = 0.007, p = 0.95, Figura 6B).
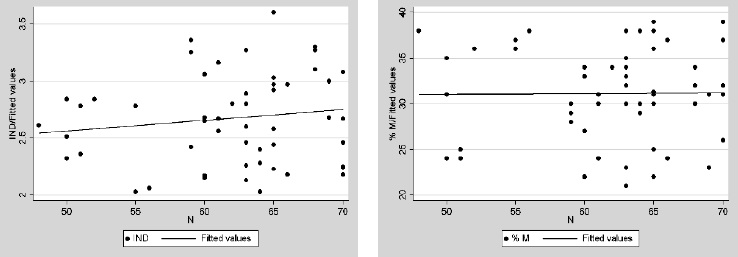
Figura 6. Correlación entre el número de PMN y el índice de fagocitosis (A) y el porcentaje de muerte intracelular de Cándida (B). N: porcentaje de neutrófilos.
En la actualidad existen técnicas que evalúan la capacidad fagocítica en los procesos infecciosos a repetición (12-14). Sin embargo, estas pruebas tienen limitaciones como la cantidad requerida de muestra sanguínea y el tiempo prolongado del proceso, que influye en los resultados por excesiva manipulación de las células (6).
Con la microtécnica de fagocitosis y muerte intracelular de Cándida, los inconvenientes anteriormente descritos son eliminados, solo se necesitan tres gotas de sangre periférica, no requiere de alta tecnología en el laboratorio y el tiempo de manipulación de las células es corto (7). Por todo lo anterior, este estudio es de gran importancia en la evaluación de la función fagocítica de los PMN, puesto que permitió la obtención de valores de referencia en un grupo de sujetos sanos de nuestro país y, adicionalmente, se constituye en un método sencillo de valoración de la función fagocítica.
En relación a la técnica, se deben tener en cuenta las siguientes consideraciones: la humedad, la temperatura (37 °C) y el pH fisiológico para no alterar las membranas celulares, debido a la poca cantidad de muestra utilizada. Estos factores podrían llegar a afectar la capacidad de adhesión al vidrio, la fagocitosis y la muerte intracelular del germen. Con la Cándida álbicans es importante tener en cuenta que se debe usar un cultivo fresco (no más de 24 horas) para no usar levaduras gemantes, puesto que en el recuento de levaduras intracelulares puede verse alterado el resultado de microorganismos fagocitados. En éste trabajo el pool de opsoninas usadas se debe almacenar a temperaturas inferiores a -70 °C.
En la población estudiada el índice fagocitosis fue de 2.70 +/- 0.43 (media +/- DE) con un rango de 2.03 a 3.92 y el porcentaje de muerte Intracelular fue de 31.31 +/-5.10 (media +/- DE) con un rango de 21 a 39%. No encontramos diferencias en la actividad fagocítica de los PMN de acuerdo con la edad a diferencia del estudio de Muniz y colaboradores, quienes encontraron que los valores de la fagocitosis están influenciados por la edad y la vía de nacimiento (cesárea o vía vaginal), factores que aún no se han esclarecido (6).
Tampoco se encontraron diferencias en la actividad fagocítica de los PMN de acuerdo con el género, el número de leucocitos o el porcentaje de PMN circulantes en la población estudiada. Esto podría indicar que la función fagocítica en sujetos sanos se cumple independientemente de esos factores.
En conclusión, consideramos que la microtécnica de fagocitosis y muerte intracelular de Cándida es una herramienta diagnóstica importante, altamente reproducible para evaluar el funcionamiento del sistema inmune innato, específicamente en la fagocitosis. Se ofrecen valores de referencia para sujetos sanos.