Efecto del Mercurius-Heel®s sobrela citotoxicidad de fibroblastos gingivales humanos en un modelo in vitro
Gabriela Rueda1, Dabeiba Adriana García1, Liliana Catherine Patiño1, Angélica Cagueñas1, Mariana García1
1Pontificia Universidad Javeriana. Centro de Investigaciones Odontológicas.
Correspondencia: garciad@javeriana.edu.co
Recibido: 03/04/2013 / Aceptado: 31/05/2013
La enfermedad periodontal es una patología de origen infeccioso, caracterizada por ocasionar secuelas destructivas al tejido de soporte del diente, y cuyo tratamiento va encaminado a la destrucción de los agentes etiológicos y a la regeneración periodontal. Una alternativa es el uso de agentes homeopáticos ya que son naturales y se administran a muy bajas concentraciones, uno de ellos es el Mercurius Heel® S como coadyuvante en enfermedades infecciosas. En este trabajo se presentan los resultados de una investigación cuyo objetivo fue evaluar el efecto del Mercurius Heel® S en la viabilidad de fibroblastos gingivales humanos, que fueron sometidos a tratamiento con Mercurius Heel® S durante 15 minutos y dos horas a concentraciones desde 300mg hasta 0.00006mg. Transcurridos esos tiempos, se retiró el tratamiento y las células fueron mantenidas durante 24, 48 y 72 horas más. Posteriormente se realizó un ensayo colorimétrico de viabilidad y proliferación celular denominado MTS de promega®
Los fibroblastos gingivales humanos tratados con Mercurius Heel® S mostraron un aumento en la proliferación celular comparada con las células no tratadas. Bajas concentraciones del medicamento 0,0001mg y 0,00006mg mostraron una mayor proliferación observando diferencias estadísticamente significativas. El tratamiento a 15 minutos mostró mejores resultados con respecto al tratamiento de 2 horas con diferencias estadísticamente significativas también. Finalmente el efecto del Mercurius Heel® se mantuvo hasta las primeras 48 horas. Considerando lo anterior, el Mercurius Heel® no presentó ningún efecto citotóxico en los fibroblastos gingivales; por el contrario, las células proliferaron, lo que sugiere su utilidad como tratamiento complementario en la enfermedad periodontal.
Palabras clave: citotoxicidad, fibroblastos gingivales, Mercurius Heel ®S, viabilidad.
Periodontal disease is pathology of infectious origin, characterized because it causes destructive consequences to the supporting tissue of the tooth, its treatment is aimed at the destruction of the etiologic agents and to the periodontal regeneration. An alternative is the use of homeo-pathic agents because they are natural and are managed to very low concentrations, one of them is the Mercurius Heel ® S as an adjunctive therapy in infectious diseases. In this work, we present the results of an investigation whose objective was to evaluate the effect of Mercurius Heel® S on the viability of human gingival fibroblasts, which were undergoing treatment with Mercurius Heel® S for 15 minutes and two hours to concentrations from 300mg to 0.00006mg. After these times, the treatment was removed and the cells were maintained for 24, 48, and 72 more hours. It was followed by a colorimetric assay for cell viability and proliferation called MTS of Promega ®.
Human gingival fibroblasts treated with Mercurius Heel® S showed an increase in cell prolife-ration compared with the untreated cells. Low medication concentrations of 0.0001 mg and 0.00006 mg showed a greater proliferation showed greater statistically differences. Finally, the effect of Mercurius Heel® was maintained for the first 48 hours. Considering the above, the Mercurius Heel® did not provide any cytotoxic effect on human gingival fibroblasts; on the contrary, the cells proliferated, suggesting its usefulness as supplementary treatment for periodontal disease.
Key Words: cytotoxicity, gingival fibroblasts, Mercurius Heel ®S, viability.
La periodontitis es una enfermedad infecciosa de etiología polimicrobiana que genera inflamación de los tejidos de soporte dental, pérdida de inserción progresiva y pérdida ósea (1-3). En Colombia, la enfermedad periodontal evaluada mediante la pérdida de inserción clínica afecta al 50,2% de la población, lo que ratifica su alta incidencia en nuestro país (2). Esta patología normalmente inicia con una gingivitis, en donde la infección bacteriana es seguida por la respuesta inflamatoria activa del huésped. Cuando la periodontitis está bien establecida conlleva a la reabsorción y pérdida de tejido, en este momento es necesario llevar a cabo un tratamiento efectivo para además de remover la placa, controlar el proceso inflamatorio con el fin de regenerar el periodonto (1).
En los últimos años, la medicina homeopática ha tomado gran fuerza debido a que es un trata-miento no invasivo basado en la administración de sustancias naturales, que en pequeñas dosis, no traen efectos secundarios y pueden ser utilizados al tiempo con los tratamientos de la medicina convencional (4-6). Sin embargo, aún existe un gran debate sobre la efectividad de estos medicamentos, pues son pocos los estudios que se han realizado donde se demuestren sus propiedades curativas (7,8). En el área odontológica por ejemplo, existen diversos tratamientos homeopáticos para múltiples patologías en las que podemos mencionar: abscesos dentales, bruxismo, sensibilidad dental, sangrado, infecciones, úlceras y traumas, entre otros (4,10).
No obstante, investigaciones donde se evidencie su efectividad son muy escasas (10), y las pocas que hay son muchas veces contradictorias (10 -13). En un estudio realizado recientemente en el Reino Unido, evaluaron la prescripción homeopática en enfermedad periodontal aguda y crónica hecha por tres odontólogos a 51 pacientes durante 18 meses, encontrando resultados positivos en cuanto a la reducción de la bolsa periodontal, sugiriendo que la homeopatía es un área promisoria en el tratamiento de la enfermedad periodontal (14).
Un medicamento homeopático promisorio para esta patología es el Mercurius Heel® S, que es in-dicado en el tratamiento de procesos infecciosos y supurativos como por ejemplo: aftas, bronquitis, cistitis, paperas, otitis y sinusitis (15-17). Su componente principal es Mercurius solubilis, prepara-do a partir de una compleja sal de mercurio (mercurio metálico, nitrato mercurioso y ácido nítrico), que puede ser tóxico a altas dosis, pero utilizado homeopáticamente puede traer enormes beneficios en el tratamiento de estas enfermedades (18,19).
Debido a sus propiedades antiinflamatorias, el Mercurius Heel® S también ha sido indicado como tratamiento complementario para gingivitis y periodontitis, sin embargo, no se han realizado estudios que muestren el efecto que tiene este medicamento sobre células orales. Con el fin de dar una explicación científica al uso del Mercurius Heel® en enfermedades orales como la periodontitis, el presente estudio propone evaluar la citotoxicidad de este medicamento en Fibroblastos Gingivales Humanos (FGH). Lo cual permitirá considerar su utilización en apoyo al tratamiento convencional de la enfermedad periodontal.
Cultivo celular
Se utilizó la línea celular ATCC CRL-2014 que corresponde a FGH. Las células fueron mantenidas de acuerdo a las recomendaciones dadas por el fabricante, en medio Dulbecco’s modified Eagle’s medium (DMEM) (GIBCO) suplementado con 10% de suero fetal bovino (GIBCO), 100 U/ml de penicilina y 100 g/ml de estreptomicina (GIB-CO). Las células fueron incubadas a 37° C, 5% de CO2 y 100% de humedad relativa. Cuando las células lograron confluencia al 80% se realizaron pases por desprendimiento con tripsina 0,25% Y EDTA 1mM (GIBCO) a 37° C durante 2 minutos. Transcurrido ese tiempo se inactivó la tripsina con medio DMEM suplementado y se centrifugó durante 5 minutos a 2000 rpm.
Tratamiento con Mercurius Heel®S
El peso de cada tableta de Mercurius Heel®S fue de 300 mg, con ayuda de un triturador de pastillas de Acu-Life® se trituraron 2 tabletas que fueron disueltas en medio DMEM suplementado para lo-grar las concentraciones evaluadas de 300 mg/ml a 0,00006 mg/ml, realizando diluciones en base de 3.
Viabilidad celular
El efecto del Mercurius Heel®S, en la viabilidad de FGH, fue evaluado mediante el uso del kit Cell-Titter 96 AQueous (PROMEGA) y el espectrofotómetro Humareader, en ensayos por triplicado. Los FGH fueron sembrados en placas de 96 pozos a una concentración de 5x103 células por pozo. Se permitió su adherencia durante 24 horas después de sembradas, se cambió el medio y se aplicaron concentraciones de 300mg/ml a 0,00006 mg/ml de Mercurius Heel® S. A tres pozos no se les agregó el medicamento y se usaron como control. Al cumplir con el tiempo de exposición al medicamento (15 minutos y 2 horas), se retiró el tratamiento y se cambió el medio a DMEM suplementado y se incubó por 24, 48 y 72 horas más. En cada uno de estos tiempos se adicionó el cell titer de acuerdo a las recomendaciones dadas por el fabricante. Final-mente las placas fueron leídas en el espectrofotómetro a 490nm. Los datos fueron promediados por triplicado y se calculó el porcentaje de proliferación celular tomando como el 100% el valor obtenido para el control.
Análisis estadístico
Se utilizó el programa Graphpad, y las pruebas es-tadísticas que se hicieron fueron: inicialmente la prueba de Shapiro Wilk para evaluar la normali-dad de las variables, esto con el objetivo de estar seguros de que se podían comparar los promedios. Posteriormente se compararon los promedios entre cada uno de los grupos a través de la prueba one way ANOVA y comparación entre grupos con la prueba de Tukey´s para grupos independientes. Fi-nalmente se compararon los tratamientos a los 15 minutos y 2 horas mediante t- test.
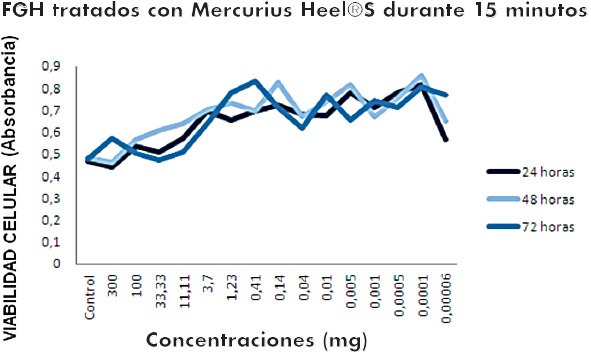
La viabilidad de los FGH tratados con Mercurius Heel® S no mostró ningún tipo de citotoxicidad a ninguna de las concentraciones y tiempos evalua-dos. Los resultados de los diferentes grupos mos-traron una distribución normal (p>0,05), por lo cual se evaluaron las diferencias estadísticamente significativas con one-way ANOVA y Tukey’s test. A los 15 minutos de tratamiento con Mercu-rius Heel® S, se observa que la viabilidad celular se incrementa en las diferentes concentraciones en referencia a las células sin tratamiento (con-trol) (Figura 1).

Figura 1. Viabilidad de FGH tratados con Mercurius Heel® S durante 15 minutos y evaluados a las 24, 48 y 72 horas después de retirado el tratamiento
Las concentraciones en donde se observa mayor pro-liferación celular fueron entre 3,7 mg a 0,00006 mg, lo que nos indica que a bajas concentraciones de Mercurius Heel® S se evidencia su mayor efecto, observándose diferencias estadísticamente significativas entre el grupo control y las concen-traciones de 0.0001 y 0.00006 mg de Mercurius Heel® S. Con respecto a las horas de recuperación de las células a las 24, 48 y 72 horas no se observan diferencias estadísticamente significativas p=0.69.
En referencia al tratamiento con Mercurius Heel® S a las 2 horas sobre FGH, se observa un comportamiento similar al del tratamiento de 15 minutos, ya que hubo un incremento de la viabilidad a todas las concentraciones del tratamiento incluidas las más bajas (Figura 2). Al comparar el control con los diferentes tratamientos se observa diferencias estadísticamente significativas con la concentración de 0,01mg y las concentraciones elevadas de 300mg a 33.33mg, también se ob-servaron diferencias estadísticamente significa-tivas con las concentraciones de 0,00006mg de Mercurius Heel ®-S. Con respecto a las horas de recuperación las células mostraron que tanto a las 24, 48 y 72 horas el comportamiento aunque es similar, se encontraron diferencias estadísti-camente significativas entre 24 horas y 72 horas p=0.049.
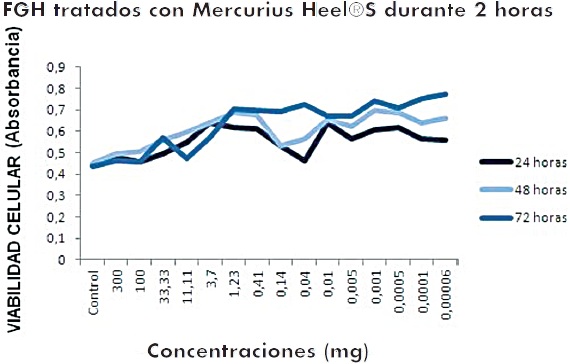
Figura 2. Viabilidad de FGH tratados con Mercurius Heel® S durante 2 horas y evaluados a las 24, 48 y 72 horas después de retirado el tratamiento
Al realizar una comparación entre el tratamien-to de Mercurius Heel ®-S a los 15 minutos y 2 horas, se observó que los resultados obtenidos, luego de 15 minutos de tratamiento, muestran una mayor proliferación celular con respecto a las 2 horas (Figura 3 A-C). A las 24 y 48 horas se observaron diferencias estadísticamente signi-ficativas p=0.009 y p=0.0048 respectivamente entre estos dos grupos de tratamiento, mientras que a las 72 horas no se observaron diferencias estadísticamente significativas p=0.12. Estos resultados sugieren que a corto tiempo el trata-miento en contacto las células es suficiente para obtener buenos resultados. Lo que de cierta for-ma puede indicar que la tableta de Mercurius Heel® S el tiempo que tarda en disolverse en boca (aproximadamente 15 minutos) es suficiente para su mejor y mayor resultado.
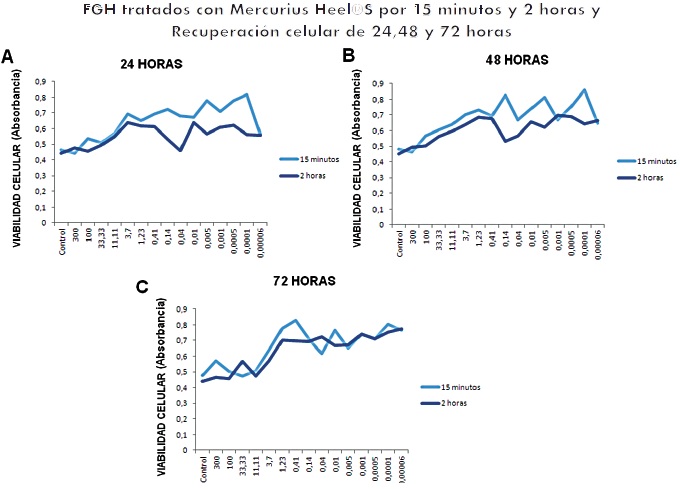
Figura 3. Viabilidad de FGH tratados con Mercurius Heel® S durante 15 minutos y 2 horas y evaluados a los diferentes tiempos luego de retirado el tratamiento A. 24 horas B. 48 horas y C. 72 horas
La presente investigación se planteó con el fin de determinar el efecto del Mercurius-Heel-S® sobre la viabilidad de los FGH cultivados in vitro; con el fin de analizar su posible uso como parte del tra-tamiento de la enfermedad periodontal. El Mercu-rius solubilis es el mayor componente del Mercurius Heel®; es extraído del cinabrio, también conocido como cinabrita, compuesto en un 85 % por mercu-rio, presente en fuentes termales y volcanes.
En un estudio realizado por De Oliveira y colabo-radores evaluaron el efecto del Mercurius solubilis en macrófagos peritoneales en ratones in vivo e in vitro, como células capaces de modular la respuesta inmune, observando que a muy bajas concentracio-nes del Mercurius, la respuesta del macrófago, en cuanto a citoquinas y especies reactivas de oxígeno y nitrógeno, se incrementaba, indicando una acti-vación en la respuesta inmune e inflamación por aumento del óxido nítrico y la producción IFNγ, sin embargo, naturalmente luego de la eliminación del agente causal de la inflamación, es necesario la activación de la respuesta antiinflamatoria como la IL4, la cual observaron que también se incremen-taba, sugiriendo que el Mercurius solubilis es capaz de modular la respuesta del macrófago induciendo un balance y homeóstasis entre una respuesta pro-inflamatoria y anti-inflamatoria (18).
Otro estudio realizado en animales, específica-mente en ratas Wistar, evaluaron el efecto del Mercurius solubiis en alveolitis, determinando que el grupo manejado con el medicamento homeopático mantuvo una microbiota dentro de los parámetros normales, obteniendo su mejor efecto a los 21 días de tratamiento, a diferencia de los otros grupos que no recibieron tratamiento, los cuales mostraron números incrementados de pa-tógenos (20).
En la presente investigación, uno de los principales hallazgos fue el aumento de la proliferación celu-lar. Se observó que el Mercurius Heel® no presentó ningún efecto citotóxico en los fibroblastos gingi-vales, al utilizar concentraciones entre 300mg (una tableta) a 0,00006mg. Al igual que en el estudio de Oliveira, también se obtuvo mejores resultados en concentraciones bajas del medicamento, lo que favorece lo descrito por la homotoxicología, donde se considera que cuanto más diluido esté un medi-camento homeopático, más potentes es.
Por otra parte, también se estableció que un cor-to periodo de tiempo (15 minutos) es suficien-te para obtener buenos resultados, tiempo en el cual la tableta se disuelve en la boca, además su efecto puede observarse hasta 48 horas después de ejercido el estímulo. Finalmente, gracias a los resultados de esta investigación se puede sugerir que el Mercurius Heel® puede ser usado como adyuvante o complemento al tratamiento de la enfermedad periodontal, por ser esta una pato-logía con un alto componente infeccioso y del huésped principalmente asociado a respuesta inmunológica, ya que este medicamento puede regular la respuesta inmune frente a patógenos y no causa un efecto letal o dañino a las células del hospedero e incluso promueve proliferación celular, lo que indica su potencial uso en regene-ración periodontal.
A la Pontificia Universidad Javeriana por su apoyo financiero y al Centro de Investigaciones Odonto-lógicas por sus instalaciones para la realización del presente estudio.
1. Chen FM, Jin Y. Periodontal tissue engineering and regenera-tion: current approaches and expanding opportunities. Tissue Eng Part B Rev 2010; 16: 219-255.
2. Fayad I, Lafaurie G, Contreras A, Castillo D, Barón A, Aya M. Microflora subgingival en periodontitis crónica y agresiva en Bogotá, Colombia: un acercamiento epidemiológico. Biomé-dica 2007;27:21-33.
3. Herrera D, Contreras A, Gamonal J, Oteo A, Jaramillo A, Silva N, Sanz M, Botero JE, León R. Subgingival microbial profiles in chronic periodontitis patients fron Chile, Colombia and Spain. J Clin Periodontol 2008;35: 106-113.
4. Shaw D. Unethical aspects of homeopathic dentistry. Br Dent J. 2010;209:493-6.
5. Rutten AL. Comparison of effectiveness of frequently and infrequently used homeopathic medicines. Homeopathy. 2011;100:175-82.
6. Clausen J, van Wijk R, Albrecht H. Review of the use of high potencies in basic research on homeopathy. Homeopathy. 2011;100:288-92.
7. Novella S, Roy R, Marcus D, Bell IR, Davidovitch N, Saine A. A debate: homeopathy--quackery or a key to the future of medicine? J Altern Complement Med 2008;14: 9-15.
8. Gold PW, Novella S, Roy R, Marcus D, Bell I, Davidovitch N, Saine A. Homeopathy--quackery or a key to the future of medicine? Homeopathy 2008;97:28-33.
9. Eames S, Darby P. Homeopathy and its ethical use in dentis-try. Br Dent J. 2011;210:299-301.
10. Mathie RT, Farrer S. Outcomes from homeopathic prescri-bing in dental practice: a prospective, research-targeted, pilot study. Homeopathy. 2007;96:74-81.
11. Kaziro GS. Metronidazole (Flagyl) and Arnica Montana in the prevention of post-surgical complications, a comparative placebo controlled clinical trial. Br J Oral Maxillofac Surg. 1984;22:42-9.
12. Lökken P, Straumsheim PA, Tveiten D, Skjelbred P, Borch-grevink CF. Effect of homoeopathy on pain and other events after acute trauma: placebo controlled trial with bilateral oral surgery. BMJ. 1995;310:1439-42.
13. Haila S, Koskinen A, Tenovuo J. Effects of homeopathic treatment on salivary flow rate and subjective symptoms in patients with oral dryness: a randomized trial. Homeopathy. 2005;94:175-81.
14. Farrer S, Baitson ES, Gedah L, Norman C, Darby P, Mathie RT. Homeopathic prescribing for chronic and acute periodon-tal conditions in 3 dental practices in the UK. Homeopathy.
En prensa.
15. Sinha MN, Siddiqui VA, Nayak C, Singh V, Dixit R, Dewan D, Mishra A. Randomized controlled pilot study to compare Homeopathy and Conventional therapy in Acute Otitis Me-dia. Homeopathy. 2012;101:5-12.
16. Nayak C, Singh V, Singh VP, Oberai P, Roja V, Shitanshu SS, Sin-ha MN, Deewan D, Lakhera BC, Ramteke S, Kaushik S, Sarkar S, Mandal NR, Mohanan PG, Singh JR, Biswas S, Mathew G. Homeopathy in chronic sinusitis: a prospective multi-centric ob-servational study. Homeopathy. 2012;101:84-91.
17. Mousavi F, Mojaver YN, Asadzadeh M, Mirzazadeh M. Ho-meopathic treatment of minor aphthous ulcer: a randomized, placebo-controlled clinical trial. Homeopathy. 2009;98:137-41.
18. De Oliveira SM, de Oliveira CC, Abud AP, Guimarães Fde S, Di Bernardi RP, Coletto EL, Buchi Dde F. Mercurius solubilis: actions on macrophages. Homeopathy. 2011;100:228-36.
19. Almirantis Y. Homeopathy--between tradition and modern science: remedies as carriers of significance. Homeopathy. 2013;102:114-22.
20. de Araújo FR, de Castro CM, Severo MS, Diniz Mde F, Viana MT, Evêncio LB. Effect of Mercurius solubilis on the bacte-riological response in the alveolitis process in rats. Homeo-pathy.2009; 98:160-4.