Frecuencia de enterobacterias nosocomiales productoras de b-lactamasas de espectro extendido, Cumaná, Venezuela
Luzmila Sofía Albarado Ysasis1, José García2, Eliosmar Rodríguez2, Carmen Carpio1, Elsa Salazar3, Evelin Margarita Flores Fernández1, José Gregorio Betancourt4, Yasmina Araque Calderón3, Militza Guzmán Lista3.
1Docente Categoría Agregado.
2 Licenciado en Bioanálisis
3Docente Categoría Asociado.
4Docente Categoría Asistente. Universidad de Oriente, Núcleo de Sucre, Escuela de Ciencias, Departamento de Bioanálisis.
Correspondencia: luzalv@hotmail.com
Recibido: 25-03-09 / Aceptado: 27-05-09
El 51,42% de cultivos positivos se presentó en muestras de secreciones. Klebsiella pneumoniae mostró una frecuencia de 20/35 (57,14%). Sólo 27/35 aislados (77,14%) produjeron b-lactamasas de espectro extendido y Klebsiella pneumoniae fue la especie más frecuente en la producción de éstas, con 14/35 (40,0%). Las enterobacterias expresaron mayor porcentaje de resistencia a ceftazidima (77,77%), cefotaxima (70,37%) y cefepima (40,74%). K. pneumoniae y E. coli, mostraron 59,25% de resistencia a amoxicilina/ácido clavulánico.
Todas presentaron 100% de sensibilidad a carbapenemas. Los largos períodos de hospitalización constituyen uno de los principales factores de riesgo para adquirir infecciones intrahospitalarias y la aparición de cepas productoras de b-lactamasas de espectro extendido resultan del mal uso de cefalosporinas de amplio espectro, lo cual plantea retos importantes por la necesidad de usar carbapenemas con el riesgo de ejercer una presión selectiva que cause, a futuro, su resistencia.
Palabras clave: b-lactamasas, cefalosporinas, enterobacterias, infecciones nosocomiales, susceptibilidad antimicrobiana.
This study aimed to evaluate the frequency of nosocomial enterobacterial b-lactamase producing extended spectrum in patients confined in the Hospital Universitario “Antonio Patricio de Alcalá, Cumana, Venezuela, during the period September-November 2005. The production of b-lactamases and extended spectrum in vitro antimicrobial susceptibility were determined by the method of double-disk synergy and disk diffusion. It took 35 bacterial isolates and the increased number of nosocomial infections occurred in the intensive care unit and neonatology with 13/35 (37.15%) and 9 / 35 (25.72%) cases respectively. 51.42% of positive cultures occurred in samples of secretions. Klebsiella pneumoniae showed a frequency of 20/35 (57.14%). Only 27/35 isolates (77.14%) produced β-lactamases and extended spectrum Klebsiella pneumoniae was the most common species in the production of these, with 14/35 (40.0%). Enterobacteriaceae expressed greater percentage of resistance to ceftazidime (77.77%), cefotaxime (70.37%) and cefepime (40.74%). K. pneumoniae and E. coli, showed 59.25% resistance to amoxicillin / clavulanate. All showed 100% sensitivity to carbapenems.
Long periods of hospitalization are major risk factors for acquiring nosocomial infections and the emergence of strains producing b-lactamases extended spectrum result from misuse of broad-spectrum cephalosporins, which poses significant challenges for the need to use carbapenems with the risk of exerting a selective pressure which in time will cause future resistance.
Keywords: antimicrobial susceptibility, b-lactams, cephalosporins, enterobacteria, nosocomial infectionsenterobacterial.
El amplio uso de los antibioticos, el incremento de la expectativa de vida, incluso en pacientes con enfermedades cronicas y la aparicion de la unidad de cuidados intensivos (UCI), son factores que inciden directamente en la resistencia bacteriana a los antimicrobianos, y en el aumento de las IIH (4). Herrera y colaboradores señalan que este aspecto representa un problema de salud publica de caracter global (no existiendo pais exento a este impacto) y una situacion promovida, basicamente, por el uso indiscriminado de antibioticos en hospitales, clinicas, comunidad, agricultura y produccion de alimentos (5).
Se conocen al menos siete mecanismos diferentes de resistencia a antimicrobianos, entre las enzimas mas frecuentes que confieren resistencia estan las b-lactamasas (6). La clasificacion mas utilizada para la nomenclatura de estas enzimas, ha sido la propuesta por Bush, Jacoby y Medeiros; el grupo 2b de esta clasificacion, incluye las enzimas TEM-1, TEM-2 y SHV-1, conocidas como b-lactamasas de espectro extendido (BLEE), su presencia y permanencia en las bacterias es debido a la elevada presión selectiva ejercida por el uso irracional de la ampicilina, carbenicilina y CF1G (7-9). Adicional a las enzimas TEM y SHV, ha aparecido un nuevo grupo de BLEE, conocidas como cefotaximasas (CTX-M), las cuales presentan un grado de homologia a nivel nucleotidico con TEM y SHV de 40% (10). El Clinical and Laboratory Standards Institute (CLSI) sugiere evaluar agentes antimicrobianos como aztreonam, cefpodoxima, ceftazidima, cefatoxima y ceftriazona para realizar la deteccion de BLEE y confirmar la producción de estas enzimas en presencia de un agente inhibidor (11).
El acido clavulanico (AC) es un excelente inhibidor de las BLEE, usado al disenar metodos para detectarlas al producir un fenomeno sinergico entre CF3G, por ejemplo ceftazidima o cefotaxima y AC en ensayos por difusión en agar usando discos con estos compuestos (12). El uso indiscriminado de CF3G en los centros hospitalarios, ha favorecido la aparicion de importantes brotes nosocomiales causados por enterobaterias productoras de BLEE. La deteccion precoz de estas cepas y la aplicacion de medidas de control adecuadas, favorecen la erradicacion y vigilancia de estos brotes nosocomiales (13).
Se planteo como objetivo evaluar la frecuencia de enterobacterias nosocomiales productoras de BLEE en pacientes recluidos en el Servicio Autonomo Hospital Universitario “Antonio Patricio de Alcala (SAHUAPA), en el periodo septiembre- noviembre de 2005.
El estudio bacteriologico se realizo siguiendo lineamientos de Koneman y su equipo (15) para la identificacion de enterobacterias. A partir del medio de conservacion, las cepas bacterianas se inocularon en caldo infusion cerebrocorazon, BHI (Himedia), y se incubaron por 24 horas a 37oC en aerobiosis. Luego, se sembraron en agar tripticasa de soya, ATS (Himedia) y agar MacConkey, AMC (Himedia), incubandose en iguales condiciones (16). La evaluación macroscopica de las colonias se realizo por observacion de sus caracteristicas morfologicas y cambios producidos en el AMC (15). El estudio microscopico, se realizo preparando un extendido a partir del cultivo en ATS, luego, se procedio a colorear con el metodo de Gram (17), para establecer morfologia y tincion bacteriana. La caracterización bioquimica de las cepas se realizo segun protocolos de identificacion convencional para bacterias Gram negativas fermentadoras y no fermentadoras de lactosa, propuestos por Koneman y colaboradores (15) y Mac Faddin (16).
La susceptibilidad antimicrobiana fue realizada mediante el metodo de difusion del disco (18), siguiendo los lineamientos propuestos para enterobacterias por el CLSI (11), empleando discos de antibioticos de la casa comercial OXOID: amoxacilina-acido clavulanico 2:1 (20 μg/10 μg), cefotaxima (30 μg), ceftazidima (30 μg), cefepima (30 μg), imipenem (10 μg), meropenem (10 μg).
Los resultados se reportaron segun recomendaciones del CLSI (11) en las categorias de interpretacion de acuerdo a los datos obtenidos in vitro (19).
La produccion de BLEE se determino por la técnica de sinergismo de doble disco propuesta por Jarlier y colaboradores (20) y siguiendo los lineamientos establecidos por CLSI (11), M100-S15 (M2), aplicándose a las cepas recolectadas de Klebsiella spp, E.coli y también a Enterobacter spp. Para ello, se coloco en el centro de una placa de agar Mueller Hinton (DIFCO) un disco de amoxacilina/acido clavulanico 2:1 (20 μg/10 μg) y los discos de ceftazidima y ceftriazona a una distancia lineal de 20 mm del disco central en un angulo de 90o, a 20 mm del mismo se ubicaron los discos de aztreonam y cefotaxima.
La formacion de un ovalo en la zona de conversion del halo de inhibicion de los agentes antimicrobianos empleados y el disco central de amoxacilina-acido clavulanico y la sensibilidad ante cefoxitina, es indicativo, desde el punto de vista fenotipico, de la presencia de BLEE. La calidad de los discos de antibioticos, asi como la produccion de b-lactamasas, fue controlada empleando las cepas de E. coli ATCC 25922, especie BLEE negativa, y K. pneumoniae ATCC 700603, productora de BLEE (11).
Para establecer la frecuencia de bacterias productoras de BLEE, se empleo un analisis porcentual. Asimismo, se aplico un analisis de multiples variables para correlacionar las enterobacterias nosocomiales identificadas, producción de BLEE, tiempo de estadia en el centro hospitalario, tipo de muestra analizada y area de hospitalizacion, a un nivel de confiabilidad de 95% (21).
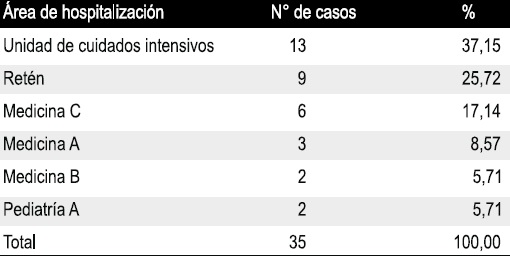
Tabla 1. Distribución porcentual del número de casos de infecciones nosocomiales
causadas por enterobacterias, según las áreas de hospitalización.

Servicio Autónomo Hospital Universitario “Antonio Patricio de Alcalá”, Cumaná, Venezuela. Septiembre noviembre de 2005.
Tabla 2. Frecuencia de cultivos positivos para enterobacterias nosocomiales, según el tipo
de muestra clínica.
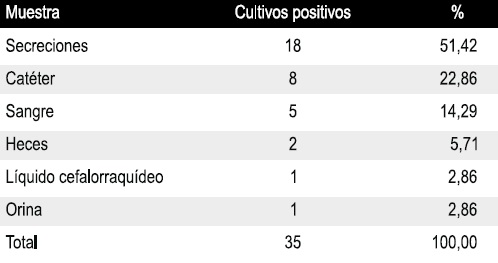
Servicio Autónomo Hospital Universitario “Antonio Patricio de Alcalá”, Cumaná, Venezuela. Septiembre noviembre de 2005.
La deteccion fenotipica de BLEE indico que de 35 aislados bacterianos, 27 fueron productores de estas enzimas, lo que representa 77,14%, la produccion en K. pneumoniae fue 14/20, correspondiendose con 40,00%, seguido de E. aerogenes, donde 5 aislados resultaron productores con 14,29%, Tabla 4.
Tabla 3. Frecuencia de enterobacterias nosocomiales.
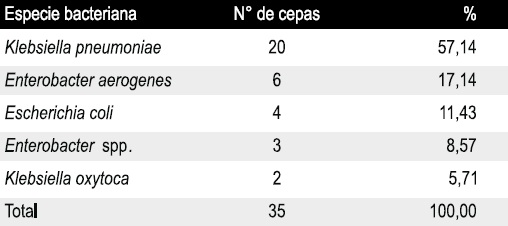
Servicio Autónomo Hospital Universitario “Antonio Patricio de Alcalá”, Cumaná, Venezuela. Septiembre noviembre de 2005.
Tabla 4. Frecuencia de enterobacterias nosocomiales productoras de b-lactamasas de espectro expandido
Servicio Autónomo Hospital Universitario “Antonio Patricio de Alcalá”, Cumaná, Venezuela. Septiembre-noviembre de 2005. BLEE: b-lactamasas de espectro expandido.
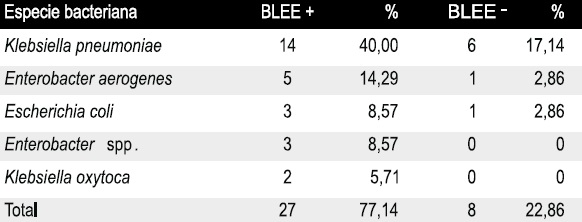
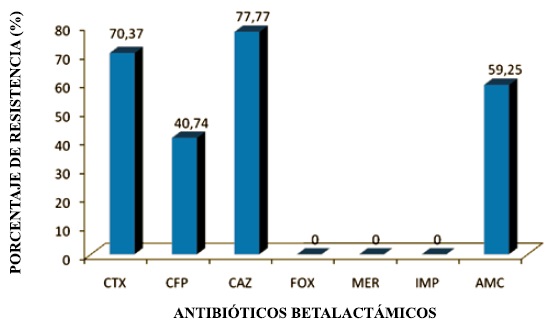
Figura 1. Susceptibilidad in vitro a los antibacterianos b-lactámicos. CTX: cefotaxima, CFP: cefepima;
CAZ: ceftazidima, FOX: cefoxitina (excepto Enterobacter spp.), IPM: imipenem, MER: meropenem, AMC: amoxicilina/ácido clavulánico (sólo para K. pneumoniae y E. coli).
Las pruebas de susceptibilidad in vitro a los antibacterianos b-lactamicos muestran que las enterobacterias nosocomiales expresaron mayor porcentaje de resistencia a ceftazidima con 77,77% y a cefotaxima con 70,37%. En la Figura 1 se muestra el porcentaje de susceptibilidad a los antibioticos b-lactamicos.
Alpuche y Daza (23) en un estudio sobre frecuencia de bacterias nosocomiales resistentes a cefalosporinas de espectro extendido, mostro que entre 35 y 40% de las IIH procedian de UCI. Perez publico que las UCI representan, en muchos casos, el recurso mas idoneo para salvar la vida de los pacientes en estado critico, sin importar la causa de su ingreso, pero esaesperanza de vida tiende a complicarse dado que las UCI estan propensas a albergar microorganismos causantes de infeccion nosocomial (24).
Este estudio mostro un 51,42% de cultivos positivos para enterobacterias nosocomiales a partir de secreciones. Resultados relacionados fueron publicados por Poveda y su equipo (25), quienes en un estudio sobre infecciones nosocomiales en terapia intensiva, mostraron un 79% de cultivos positivos en secreciones. K. pneumoniae fue la especie bacteriana mayormente aislada (57,14%). Estos resultados guardan relacion con un trabajo realizado por Poveda y colaboradores (25), donde Klebsiella pneumoniae fue el principal agente causal de IIH (33,30%). Cornejo y colaboradores (28), en Mexico, publicaron una investigacion sobre patrones de resistencia bacteriana en urocultivos, analizando por separado cepas nosocomiales y de la comunidad, E. coli ocupo el primer lugar en muestras nosocomiales con 41,3%.
En este estudio se obtuvo un 77,14% de enterobacterias nosocomiales productoras de BLEE; Klebsiella pneumoniae resulto el principal productor de las enzimas. El mayor porcentaje de aislados bacterianos resistentes a antimicrobianos b-lactamicos, se obtuvo para ceftazidima (77,37%), cefotaxima (70,37%) y cefepima (40,74%), siendo totalmente sensibles a las carbapenemas ensayadas. Perozo-Mena y colaboradore (29) estudiando BLEE en cepas de E. coli y K. pneumoniae aisladas en pacientes de UCI en un hospital de Maracaibo-Venezuela, obtuvieron que 16/46 (39,02%) cepas de E. coli y 31/59 (52,54%) de K. pneumoniae resultaron positivas a la prueba en un total de 100 cepas evaluadas.
Araya y su equipo (30) en una publicacion sobre infecciones por bacterias Gram negativas en pacientes internados en el Hospital San Juan de Dios de Costa Rica, indicaron como principales agentes bacterianos a E. coli y K. pneumoniae, destacando entre los b-lactamicos, una alta resistencia a piperacilina-tazobactam (78%) y cefepima (100%), y solo el imipenem fue activo (100%) en los aislamientos. Por otro lado, Torres y colaboradores (31) en un estudio sobre BLEE en enterobacterias aisladas en Centros de Salud de Caracas, Venezuela, reportaron que de 91,10% de las cepas productoras de BLEE, 5,80% mostraron resistencia a cefepima, destacando que debido a que las BLEE sufren del efecto inoculo, en aquellas infecciones con inoculos bacterianos elevados, cefepima puede ser hidrolizada con mayor afinidad y velocidad, conduciendo a un fracaso terapeutico. Enterobacter spp., al igual que Citrobacter freundii, Morganella morganii, Providencia stuartii y Providencia rettgeri, producen b-lactamasas cromosomicas inducibles denominadas AmpC, no inhibidas por acido clavulanico y otros inhibidores de b-lactamasas (32).
Las bacterias productoras de estas enzimas son resistentes a las aminopenicilinas y a las cefalosporinas de primera, segunda y tercera generacion. La resistencia a cefoxitina varia entre las distintas especies y depende del nivel de expresion de la enzima cromosomica. En algunos casos la hiperproduccion de estas enzimas puede otorgar resistencia a dichas cefalosporinas (33). Cortes y colaboradores defienden que el factor de riesgo que mas se asocia con la produccion de BLEE es el tiempo prolongado de hospitalizacion, bien sea en un servicio medico quirurgico o en la UCI, o el antecedente de hospitalizacion y el uso previo de multiples esquemas de antibioticos, particularmente, CF3G, trimetoprim sulfametoxazol y aminoglucosidos, tambien senalan, que la presion selectiva que ha llevado a la evolucion de las BLEE ha sido usualmente atribuida al uso amplio e indiscriminado de las CF3G (34). Segun Torres y su equipo, la presencia de plasmidos de alto peso molecular en las bacterias sugiere que la presion ejercida por el uso de antibioticos en áreas como UCI, ha favorecido la diseminacion y prevalencia no solo de plasmidos transferibles, sino de otros elementos geneticos como transposones e integrones que codifican altos niveles de resistencia (31). Esto pudiera estar diseminandose facilmente entre los aislados bacterianos que producen IIH en las distintas areas del centro asistencial, probablemente, debido al excesivo uso de b-lactamicos de amplio espectro.
Los largos periodos de hospitalizacion constituyen uno de los principales factores de riesgo para adquirir IIH, el uso de antibioticos s-lactamicos es muy utilizado para su tratamiento, por su baja toxicidad y amplio espectro; sin embargo, la aparicion de cepas productoras de BLEE, resultan del mal uso de cefalosporinas de amplio espectro que ejercen una presion selectiva y favorecen la aparicion de mecanismos de resistencia, lo cual plantea retos importantes desde el punto de vista terapeutico, ya que la unica opción seria el uso de carbapenemas, con el riesgo de ejercer una presion selectiva que desarrolle su resistencia.
2. Casellas J. Resistencia bacteriana por producción de b-lactamasas de espectro extendido: La perspectiva global y latinoamericana en el escenario hospitalario. Reunión de consenso-La aparición de microorganismos productores de ESBL en América Latina: Recomendaciones para su control y tratamiento (Sao Pablo, Brasil). Infec Dis Clin Pract. 2001;12-16.
3. Díaz R, Solórzano F, Padilla G, Miranda M, González R, Trejo J. Infecciones nosocomiales. Experiencia en un hospital pediátrico de tercer nivel. Salud Púb Mex. 2001;41:12-17.
4. Owens R y Rice L. Hospital-based strategies for combating resistance. Clin Infect Dis. 2006;42:S173-181.
5. Herrera K, Espinoza M, Mejía Y, Zambrano L, Silva E, Rojas J, Gadea W, Cavaría S, Hernández M, Ramírez M, Membreño J, Lara M, Saenz J, Valle S, Torrez A, Carera E, Cáceres M. Resistencia antimicrobiana en Hospitales nor-occidentales de Nicaragua. Universitas. 2007;1:27-32.
6. Goodman R. y Gilman J. Las bases farmacológicas de la Terapéutica. Novena edición. Editorial Médica Panamericana. Buenos Aires. 1999.
7. Ambler R. The structure of beta-lactamases. Philos Trans R Soc Lond B Biol Sci. 1980;289:321-331.
8. Bush K, Jacoby G, Medeiros A. A functional classification scheme for ß-lactamases and its correlation with molecular structure. Antimicrob Agents Chemother. 1995;39:1211-1233.
9. Rice L. Evolution and Clinical Importante of Extended-Espectrum b-Lactamases. Chest. 2001;119:391 396.
10. Bradford P. Extended-spectrum b-lactamases in the 21st century: characterization, epidemiology, and detection of this important resistance threat. Clin Microbiol Rev. 2001;14:933-935.
11. Clinical and Laboratory Standards Institute (CLSI). Performance Standards for Antimicrobial Susceptibility Testing; Fifteenth Informational Supplement. 2007; 25:178.
12. Blásquez J, Baquero M, Canton R, Alos I, Baquero F. Characterization of a new TEM-type b-lactamase resistant to clavulanate, sulbactam and tazobactam in a clinical isolate of Escherichia coli. Antimicrob Agents Chemother. 1993;37:2059-2063.
13. Murria P, Baron E, Jorgensen J. Manual of Clinical Microbiology. Octava edición. ASM USA. 2003.
14. Horan TC, Andrus M, Dudeck MA. CDC/NHSN surveillance definition of health care-associated infection and criteria for specific types of infections in the acute care setting. Am J Infect Control 2008;36:309-332.
15. Koneman E, Allen S, Janda W, Schreckenberger P, Washington, W. Diagnóstico Microbiológico. Quinta edición. Editorial Panamericana. 2002.
16. Mac Faddin J. Pruebas bioquímicas para la identificación de bacterias de importancia clínica. Quinta edición. Editorial Panamericana. Buenos Aires. 2003.
17. Huccker G. y Coon H. Methods of Gram Staining. Technical Bulletin New Cork State Agricultura Experimentation. 1923;93:1-
18. 18. Bauer A, Kirby W, Sherris J, Turck M. Antibiotic susceptibility testing by a standardized single disk method. Am J Clin Pathol. 1966;45:493-496.
19. Crespo M. La lectura interpretativa del antibiograma: Una herramienta para predecir la resistencia bacteriana en el laboratorio de microbiología de rutina. Colomb Med. 2002;33:179-193.
20. Jarlier V, Nicolas M, Fournier G, Philippon A. Extended broadspectrum b-lactamases conferring resistance to newer b-lactam agents in Enterobacteriaceae: hospital prevalence and susceptibility patterns. Rev Infect Dis. 1989;10:867-878.
21. Dawsen S. y Robert G. Bioestadística Médica. Editorial el Manual Moderno S.A. México DF. 1997.
22. Martín G, Carmona O, Guzmán M. Infección nosocomial II: Resistencia a ß-lactámicos y aminoglucósidos en Pseudomonas aeruginosa en centros médicos de Venezuela durante el año 2000. Rev Soc Ven Microbiol. 2003;23: 183-189.
23. Alpuche M. y Daza C. Infecciones nosocomiales por bacterias Gram negativas resistentes a cefalosporinas de espectro extendido: edan asociación de dos peligrosos enemigos. Enf Infec y Microbiol. 2002;22:192-199.
24. Pérez C. Antimicrobianos en Unidades de Cuidados Intensivos: Uso empírico. Rev chil Infectol. 2003;20:70-73.
25. Poveda L, Villamizar D, Sánchez F, Otta A, Guevara C, Jiménez M, Besso J. Infecciones nosocomiales en terapia intensiva. Antib Infect. 2005;2:40.
26. Muzachiodi M, Ferrero S. Incidencia de enterobacterias productoras de betalactamasas de espectro extendido en el Hospital Escuela José F. de San Martín. Facultad de Cs. Exactas Nat. y Agrim. Dpto. de Bioquímica. Argentina. 2005.
27. Martínez P, Mercado M, Máttar S. Determinación de b-lactamasas de espectro extendido en gérmenes nosocomiales del Hospital San Jerónimo, Montería. Colomb Med. 2003;34:130-139.
28. Cornejo P, Velásquez C, Sandoval S, Gordillo P, Volkow P. Patrones de resistencia bacteriana en urocultivos en un hospital oncológico. Salud Púb Méx. 2007;49:330-336.
29. Perozo-Mena A, Castellano-González M, Ginestre-Pérez M, Harris B. Caracterización Molecular y Detección de Betalactamasas de Espectro Extendido en Cepas de E. coli y K. pneumoniae Aisladas en las Unidades de Cuidados Intensivos de un Hospital Universitario. Kasmera. 2007;35:91-106.
30. Araya C, Boza R, Arguedas L, et al. Infecciones nosocomiales por bacterias productoras de betalactamasas de espectro ampliado: prevalencia, factores de riesgo y análisis molecular. Acta Méd Costarric. 2007;49:90-96.
31. Torres L, Gagliotta V, Torres O, Benítez M, Domínguez M, Pedroza R. b- Lactamasas de Espectro Expandido en Enterobacterias aisladas en Centros de Salud de Caracas. Rev Soc Ven Microbiol. 2006;26:190-205.
32. Livermore D. b-lactamases in laboratory and clinical resistance. Clin Microbiol Rev. 2000;8:557-584.
33. Famiglietti A, Quinteros M, Vázquez M, Marín M, Incola F, Radice M. Consenso sobre las pruebas de sensibilidad a los antimicrobianos en Enterobacteriaceae. Rev Argent Microbiol. 2005;37:57-66.
34. Cortés J, Urdaneta A, Potdevin G, Cuervo S, Bermúdez D, Molina C, Arroyo, P. Impacto de las betalactamasas de espectro extendido en pacientes con cáncer. Rev Colomb Cancerol. 2006;10:183-196