
Sensibilidad y especificidad de E-test para la determinación de susceptibilidad antimicrobiana en aislamientos clínicos de Helicobacter pylori
Marcela Rey Arévalo1, Jenny Mireya ávila Coy 1, Alba Alicia Trespalacios Rangel2, Olga Raquel Villamizar Beltrán3, William Otero Regino4, Marcela María Mercado Reyes5
1Estudiante de Bacteriología. Facultad de Ciencias. Pontificia Universidad Javeriana.
2Profesor Asociado MSc. Departamento de Microbiología. Facultad de Ciencias. Pontificia Universidad Javeriana.
3Profesor Auxiliar Esp. Departamento de Microbiología. Facultad de Ciencias. Pontificia Universidad Javeriana.
4Profesor Asociado de Medicina MD. Coordinador de Gastroenterología. Universidad Nacional de Colombia, Gastroenterólogo Clínica Fundadores. Bogotá, Colombia.
5Profesor Asistente MSc. Departamento de Microbiología. Facultad de Ciencias. Pontificia Universidad Javeriana.
Correspondencia: mmercado@javeriana.edu.co
Recibido: 20-08-08 / Aceptado: 25-11-08
Un total de 68 referencias fueron analizadas; 8 cumplieron con los criterios de inclusión. Se analizaron como medidas de resumen “overall” la sensibilidad y especificidad de la prueba del E-test. El 87% de los artículos mostraron sensibilidad de 100%, y el 75% especificidad de 100%. La medida de resumen obtenida para sensibilidad fue de 99% (IC 95% 98 - 99%) y especificidad de 98% (IC95% 97 - 99%). El test de heterogeneidad mostró estudios homogéneos en sensibilidad y especificidad (p = 0.82) (p = 0.99). Las gráficas de “Funnel Plot” revelaron asimetría. La sensibilidad (99%) y especificidad (98%) de la técnica de E-test presentó excelente acuerdo, en especial para el antibiótico claritromicina, sin embargo no existe evidencia estadísticamente significativa para concluir que más del 90% de la literatura seleccionada, reporte valores de sensibilidad y especificidad del E-test superiores al 95% comparadas con la dilución en agar.
Palabras clave: dilución en agar, E-test, Helicobacter pylori, susceptibilidad antimicrobiana.
E-Test sensitivity and specificity for determination of antimicrobial susceptibility in clinical isolation of Helicobacter pylori
Numerous methods have been developed to detect Helicobacter pylori resistance to antimicrobials. The agar dilution is the reference method recommended by the Clinical Laboratory Standards Institute. However, it is not an easy technique that could be implemented at the laboratory routine. It must have sufficient time for preparation and handling of many culture mediums with different antibiotic concentrations. For that reason, several techniques emerge as an alternative of analysis, including E-test: an agar diffusion method, which consists of a strip with an antibiotic concentration gradient, which by reading an ellipse inhibition allows knowing the minimum inhibitory concentrations (MICs). These studies’ operative characteristics were obtained by means of contingency tables. The analysis was done using the program RevMan 5®.
From a total of 68 analyzed references, 8 reached the inclusion criteria. E-test sensitivity and specificity were analyzed as overall summary measures. 87% of the articles showed 100% sensitivity, and 75% showed 100% specificity. The summary measured obtained for sensitivity was 99% (IC 95% 98 – 99%) and 98% specificity (IC95% 97 - 99%). Heterogeneity tests showed homogenous studies in sensitivity and specificity (p = 0.82)
(p = 0.99). Funnel Plot graphics showed asymmetry. E-test sensitivity (99%) and specificity (98%) showed excellent agreement, especially for claritromicine; however, there is no significant statistical evidence to conclude that more that 90% of the selected literature reports values of E-test sensitivity and specificity higher than 90% when compared to Agar dilution.
Keywords: agar dilution, antimicrobial susceptibility, E-test, Helicobacter pylori.
El tratamiento de las infecciones producidas por H. pylori puede realizarse con la combinacion de diferentes antibioticos, entre ellos claritromicina, amoxicilina, tetraciclina y metronidazol y un inhibidor de la bomba de protones que disminuye la secrecion clorhidrica del estomago. Las monoterapias no han demostrado utilidad clinica y se recomienda el empleo de terapias dobles, triples o incluso
cuadruples (4).
Los medicamentos que generan mas resistencia antimicrobiana son los nitroimidazoles (metronidazol y tinidazol), presentando una tasa de resistencia aproximada del 35% en los paises industrializados (5). En paises como Colombia, donde el uso indiscriminado de antibioticos es muy frecuente, la tasa de resistencia es mucho mayor, razón por la cual algunos grupos no utilizan este medicamento en la terapia de erradicacion contra H. pylori.
Por la anteriormente descrito uno de los factores implicados en el fallo terapeutico es la resistencia a los antimicrobianos utilizados, por lo que es de vital importancia determinar la sensibilidad antimicrobiana mediante pruebas basadas en cultivo como la difusion en disco, microdilucion en caldo, E-test y la dilucion en agar (DA). Este ultimo establecido como metodo de referencia por el National Committee for Clinical Laboratory Standards (NCCLS) y actualmente Clinical Laboratory Standards Institute (CLSI) (6). El E-test (metodo epsilometro) es altamente concordante con el metodo de referencia y su uso esta recomendado por la British Society for Antimicrobial Chemotherapy (BSAC) (7).
Las ventajas de la prueba de DA incluyen la reproducibilidad de los resultados y el desarrollo satisfactorio de la mayoria de los microorganismos de dificil crecimiento. Sin embargo, entre sus desventajas estan la compleja metodologia requerida para su desarrollo y el alto costo por prueba. Generalmente la DA no se realiza en laboratorios clinicos de rutina pero es ideal para laboratorios regionales de referencia o laboratorios de investigación que analizan un gran numero de cepas (8). En contraste, el E-test, descrito recientemente, es el metodo de elección para uso en laboratorios de rutina e investigacion y se basa
en la combinacion de las pruebas de difusion en disco y DA entregando una sofisticada pero facil y reproducible metodologia.
El tema de la reproducibilidad de las pruebas y su adecuada utilizacion es de gran importancia al momento de realizar diagnosticos certeros sobre la sensibilidad o resistencia de un microorganismo hacia los antimicrobianos, por tanto es necesario establecer si las pruebas utilizadas para tal fin reunen las condiciones necesarias para seleccionarla como prueba de rutina capaz de generar resultados confiables que ayuden a direccionar el tratamiento adecuado basado en la susceptibilidad y no en lo que se recomienda comunmente.
El presente estudio evaluo si las características operativas de sensibilidad y especificidad de la prueba E-test, eran iguales o superiores en un 95% a las del estandar de referencia DA, en al menos el 90% de la literatura cientifica seleccionada para los antibióticos mas utilizados en la terapia erradicadora de primera línea de H. pylori en Colombia (claritromicina, amoxicilina y levofloxacina). Para la realizacion de esta investigacion se llevo a cabo una revision sistematica de la literatura que permitio conocer el estado del arte mundial de las pruebas basadas en cultivo, con miras a explorar la posibilidad de implementar el E-test en nuestro pais, como prueba de rutina hospitalaria en la determinacion de resistencia a los antimicrobianos mas utilizados para la erradicación de este microorganismo.
Tabla 1. Etapas de la revisión sistemática (14)

Tabla 2. Estrategia de búsqueda en SCIENCE DIRECT, MEDLINE y MEDLINE (ebscohot)-(ovid) y librería Cochrane

Selección de artículos
Se incluyeron articulos de pruebas diagnósticas publicados entre 1995 y 2008, que determinaron la susceptibilidad de H. pylori a claritromicina, levofloxacina y amoxicilina por las tecnicas de E-test y DA. Solo se incluyeron artículos en donde fueran descritas las caracteristicas operativas de estas pruebas. No se contemplo restriccion en cuanto a las edades, tratamientos y patologias gastricas asociadas a H. pylori de los participantes asi como de las concentraciones y combinaciones de los antibioticos en estudio.
La busqueda de los estudios se realizo en las bases de datos de MEDLINE, SCIENCE DIRECT, OVID y libreria COCHRANE (CCTR) desde 1995 hasta el 2008. Ademas de la busqueda computarizada se realizo una busqueda manual en revistas de gastroenterología desde 1995. Para la indagacion se utilizo una combinación de encabezados tematicos y terminos relacionados con la deteccion de pruebas basadas en cultivos para susceptibilidad antimicrobiana de H. pylori. Las estrategias de busqueda utilizadas para todas las bases de datos se presentan en la Tabla 2.
Selección de datos
Despues de la seleccion de los articulos se sacaron de forma independiente los datos de cada estudio en un formato previamente estandarizado y revisado por expertos. De cada uno de los estudios elegidos se obtuvieron datos para el cálculo de sensibilidad, especificidad y valor predictivo positivo y negativo mediante el uso de tablas de contingencia en caso de que no fueran expuestos por los autores. La medida de resumen “overall” fue calculada con un intervalo de confianza del 95% para cada una de las caracteristicas operativas de las pruebas. El conjunto de resultados de las caracteristicas operativas de cada estudio fue analizado mediante el uso del programa RevMan 5R de la Biblioteca COCHRANE.
Evaluación de la calidad metodológica
La calidad de los articulos fue evaluada mediante el uso de una lista de chequeo basada en los parametros de las guias para usuarios de la literatura medica (14). Los items de evaluación de la calidad se muestran en la Tabla 3. Dos observadores realizaron de forma independiente la evaluacion de la calidad de los articulos, asignandole un puntaje final a cada uno de ellos. Los desacuerdos fueron resueltos con la ayuda de expertos por medio de discusion de acuerdo a los criterios establecidos.
Tabla 3. Lista de chequeo utilizada para los estudios

Análisis estadístico
Se calcularon los parametros diagnosticos de las pruebas E-test y DA para cada estudio. La variacion entre los resultados de diferentes estudios se determino con el test de heterogeneidad (Forest plot), mediante el modelo de efectos aleatorios con un alfa de 0.05 utilizando una prueba de Chi cuadrado. Para analizar hasta que punto los resultados de los diferentes estudios podian combinarse en una unica medida, se realizo la evaluacion del grado de heterogeneidad, mediante el calculo del estadistico de Q utilizando la siguiente formula: (22)
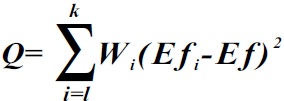
Formula: de Heterogeneidad (18).
Donde:
Efi: representa el estimador del tamaño del efecto del i-esimo ensayo.
Ef: representa el promedio de los estimadores del tamaño del efecto de los k ensayos combinados.
Wi: representa el inverso de la varianza del tamaño del efecto de i-esimo ensayo clinico (varianza de cada E).
El estadistico Q se distribuye como una funcion de distribucion ÷2 con k-1 grados de libertad y la hipótesis nula indica que los tamanos del efecto a traves de los ensayos clinicos son homogeneos (23). La exploración grafica de las caracteristicas operativas, se evaluo mediante la elaboracion de la curva ROC con sensibilidad vs 1 – especificidad y la busqueda de sesgo de publicacion se analizó mediante el uso del metodo grafico del embudo “Funnel Plot”. Los artículos excluidos se resumieron en una tabla que contenia el nombre del estudio, autor, ano de publicacion y el motivo de la exclusion.
Selección de datos
La busqueda de literatura electronica arrojo un total de 68 articulos, los cuales fueron sometidos a evaluacion por parte de expertos. De estos, 28 cumplieron los criterios de inclusion previamente establecidos. Se excluyeron aquellos articulos en los que solo se utilizaba una de las dos tecnicas evaluadas, ademas de aquellos en los que no se evaluo ninguno de los tres antibioticos en estudio (claritromicina, amoxicilina y levofloxacina). Despues de esta primera seleccion se analizaron por lectura completa cada uno de los articulos por dos evaluadores, quienes diligenciaron la lista de chequeo previamente establecida para este fin y resolvieron por discusion los posibles desacuerdos. En numero final de articulos que cumplieron estas caracteristicas fue de 8: Best, Dzieranowka, Khan, Megraud, Osato, Piccolomimi, Wang y Dore, Tabla 4 (11,15-21).
Tabla 4. Características de los estudios que comparan el E-test con la Dilución en Agar.
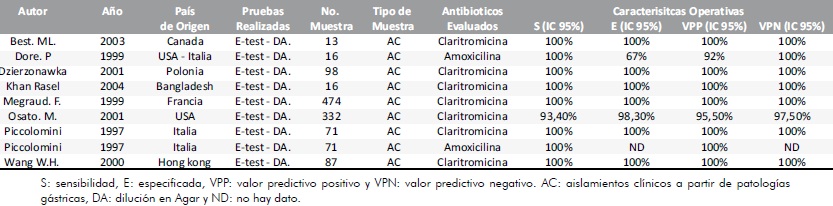
Los datos de las caracteristicas operativas (sensibilidad y especificidad) sacados de los articulos seleccionados fueron consignados en tablas de contingencia y posteriormente procesados en el programa RevMan 5R, Figura 1.
Evaluación de la calidad metodológica
La calidad de cada uno de los estudios fue valorada mediante el uso de la lista de chequeo previamente mencionada. La Figura 2 muestra que la calidad de los estudios fue buena en la mayoria de los aspectos evaluados; 7 (87%) de los estudios fueron ensayos clinicos de pruebas diagnosticas, todos compararon la prueba E-test con el patron de referencia y contenian los datos para calcular la sensibilidad y especificidad y 1 (12%) se baso en la recopilacion de datos a partir de historias clinicas. 5(62%) articulos presentaron un espectro superior al 50% y 3 no reportaron las conclusiones hechas por el autor, Figura 2.
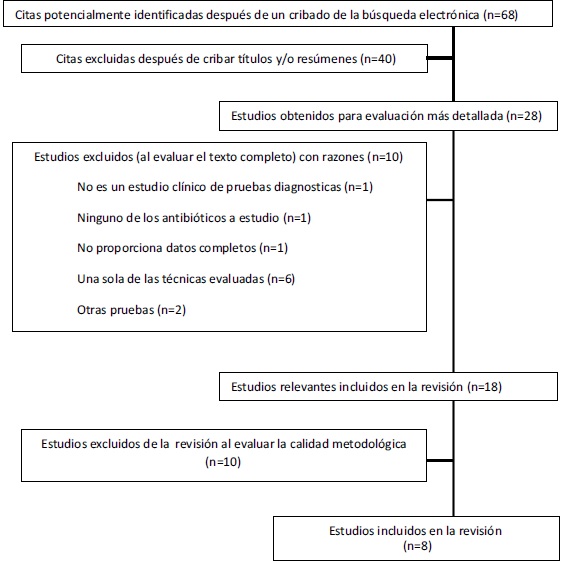
Figura 1. Selección de los estudios
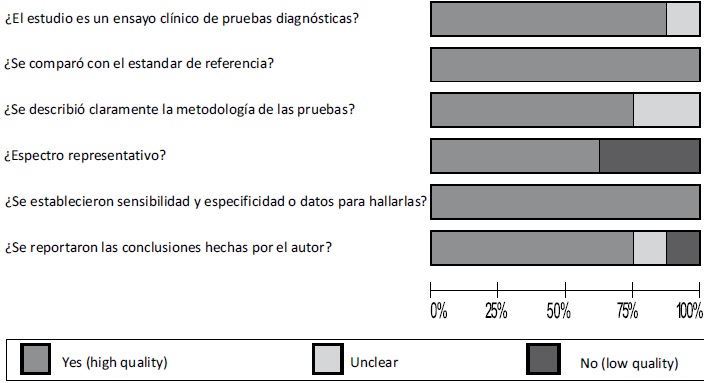
Figura 2. Evaluación de la calidad de los estudios.
Ninguno de los articulos incluidos en este estudio proporciono las caracteristicas operativas de las pruebas de forma explicita, pero si los datos para llegar al calculo de las mismas. De los 8 articulos, solo el de Piccolomini (11), para el antibiotico amoxicilina, suministro datos para sensibilidad.
Análisis de heterogeneidad
En el grafico Forest Plot se observo que el 87% de los articulos (7/8) presentaron sensibilidad de 100% y el 75% (6/8) especificidad del 100%, Figura 3. Se calculo una medida de resumen global “overall” para las características operativas, el cual entrego los siguientes datos: sensibilidad 99% (IC95% 0.98-0.99) y especificidad 98% (IC95 %0.97-0.99) p < 0,0001, Figura 3.
El calculo del estadistico Q permitio estimar el grado de heterogeneidad para las caracteristicas operativas, arrojando los siguientes valores: sensibilidad (Q=0.87; p=0.82) y especificidad (Q=7; p=0.99). Segun los datos obtenidos se observo que no existio evidencia estadisticamente significativa para afirmar que los estudios son heterogeneos.
En el 25% de los estudios (2/8) se observo una variabilidad en los intervalos de confianza entre las caracteristicas operativas para los estudios de: Rasel Khan, Shamsun Nahar, Jinath Sultana, Mian Mashhud Ahmad y Motiur Rahman (17) (29%-100%) y Maria P. Dore, Michael S. Osato, Giuseppe Realdi, Ida Mura, David Y. Graham y Antonia R. Sepulveda (21) (9%-99%), debido posiblemente al reducido tamano de muestra de los articulos relacionados.
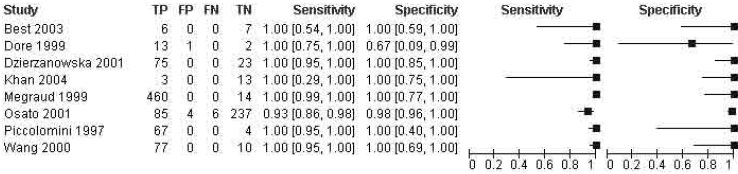
Figura 3. Forest plot: características operativas de E-test vs. Dilución en agar para todos los estudios.
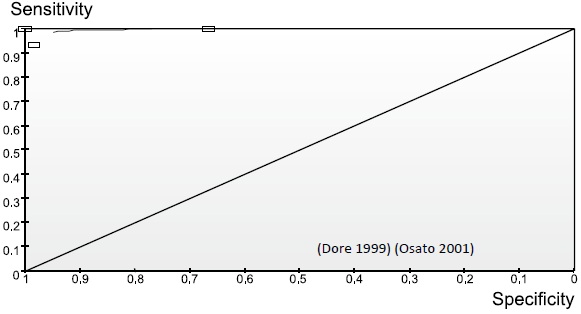
Figura 4. Curva ROC: Características operativas de E-test vs. Dilución en agar para todos los estudios.
Evaluación de las características operativas por medio de curvas ROC
En la curva ROC se observo que el 87% de los estudios (7/8) presentaron mayor area bajo la curva, esto se debio a que la sensibilidad y especificidad de estos estudios eran mayores al 95%, mientras que solo un estudio presento una especificidad baja. El estudio que mostro un menor valor de area bajo la curva fue el de Maria P. Dore y colaboradores, 2001, Figura 4 (21).
Sesgos de publicación
La presencia de sesgos en este estudio fue evaluada utilizando el grafico de embudo (Funnel Plot) (24) o tambien llamado grafico de dispersion (scatter plots). El Funnel Plot grafica el error estandar (precision de la muestra) vs la sensibilidad y la especificidad de cada estudio (tamano del efecto evaluado). El grafico de embudo mostro ausencia de simetria hacia la izquierda, lo que indica posible presencia de sesgos de publicacion, Figura 5 y 6.
Análisis por grupo antimicrobiano
En el 87% (7/8) del total de los estudios se encontró que el antibiotico de mayor investigacion para las prueba E-test y el metodo de referencia fue la claritromicina, en el grafico forest plot se observa que el 86% (6/7) de los articulos que exploraron dicho antibiotico presentaron sensibilidad y especificidad del 100%, Figura 7 El segundo antibiotico encontrado en esta revision fue la amoxicilina, con una sensibilidad del 100% para solo dos articulos. El estudio de Raffaele Piccolomini, Giovanni Di Bonaventura, Giovanni Catamo, Flavia Carbone y Matteo Neri (11) no proporciono datos que permitieran calcular especificidad y el estudio de Maria P. Dore y colaboradores (21), mostro un intervalo de confianza poco preciso, Figura 8.

Figura 5. Funnel plot para sensibilidad.
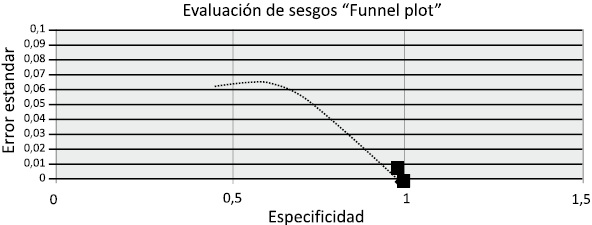
Figura 6. Funnel plot para especificida
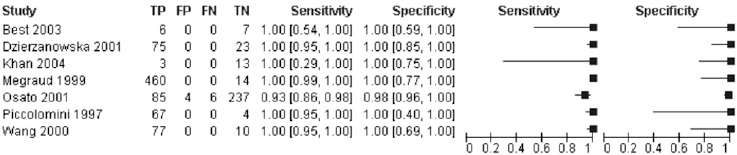
Figura 7. Características operativas E-test vs. dilución en agar para la claritromicina.

Figura 8. Características operativas E-test vs. dilución en agar para la amoxicilina.
No se encontraron estudios que exploraran las características operativas de las pruebas E-test y DA para la levofloxacina. En cuanto a la hipótesis formulada para este estudio, se demostró que no existe evidencia estadísticamente significativa para concluir que mas del 90% de la literatura seleccionada reporta valores de sensibilidad y especificidad del E-test frente a la DA superiores al 95%. (P>0.05).
Esta afirmacion debe ser demostrada en la terapia de erradicacion para H. pylori en nuestro pais antes de recomendar su uso, por tanto fue necesario realizar una revision sistematica.
Lo primero a destacar en esta revision es la escasez de publicaciones encontradas sobre este tema, tambien se observo que dichos estudios no eran recientes debido a que las pruebas utilizadas ya han sido exploradas y actualmente se utilizan de forma individual en otras regiones, razón por la cual en la mayoria de articulos excluidos solo se utilizaba la tecnica de E-test (11).
De los articulos analizados se observó que la exploración de las pruebas se realizo con pocos pacientes pero con similares disenos metodologicos y resultados muy homogeneos. La metodologia experimental utilizada en general fue la misma: medios de cultivo (Mueller Hinton suplementado con 5% de sangre de oveja), tiempos y atmosferas incubacion (72 h a 37 oC en frasco campyGen), casa comerciales (AB Biodisk – Abbott) y preparacion del inoculos (Escala de Mcfarland No. 2 o 3). La DA para todos los estudios siguio el protocolo de la NCCLS (National Committee for Clinical Laboratory Standards) actualmente CLSI (Clinical Laboratory Standards Institute) (8).
Durante la busqueda de los articulos se encontro que la claritromicina fue el antibiotico mas explorado por la prueba E-test y DA, seguido por amoxicilina. No se encontraron articulos donde se utilizaran estas técnicas para evaluacion de sensibilidad a levofloxacina, esto debido a que su uso en el tratamiento contra H. pylori no es muy frecuente y por ende su tasa de resistencia es baja (5).Por tal motivo no se pudo realizar un analisis de esta prueba.
En la busqueda tambien se observo que las pruebas motivo de este estudio se compararon con mas frecuencia para metronidazol, este antibiotico no fue contemplado en este analisis, puesto que H. pylori presenta gran resistencia a nivel mundial a este medicamento. Este antibiotico mostro baja correlacion al momento de detectar sensibilidad y resistencia entre las pruebas estudiadas, limitando aun mas la busqueda de articulos (25).
El hecho de comparar las caracteristicas operativas del E-test con la DA hace que los resultados de la prueba sean mas confiables y validos al momento de detectar susceptibilidad antimicrobiana, puesto que sus resultados estan respaldados con una prueba, que aunque de dificil manipulacion, proporciona excelentes datos de sensibilidad y resistencia para microorganismos de difícil crecimiento (independiente de su desenlace).
Ninguno de los estudios incluidos en el trabajo proporciono datos expuestos en valores de sensibilidad y especificidad de las dos pruebas, por lo tanto fue necesario calcularlos. Sin embargo, un artículo que evaluaba la susceptibilidad a amoxicilina, no permitio calcular la especificidad debido a que no se suministró el valor total de cepas resistentes, es decir los verdaderos negativos para ambas pruebas. Aunque la amoxicilina presento buena correlacion entre las pruebas para sensibilidad, no se encontro suficiente literatura que confirmara esta afirmación.
En la mayoria de los estudios se observó que el antibiotico de mayor exploracion en esta revision y que presento las mejores caracteristicas operativas fue la claritromicina 7/8 (87%); sin embargo, los datos no fueron estadisticamente significativos para recomendar completamente el uso de esta prueba, esto quiere decir que el E-test mostro buenas caracteristicas operativas pero no supera las del metodo de referencia.
El estudio de Maria Dore y colaboradores (21) a pesar de suministrar una sensibilidad del 100%, presento una especificidad del 67%, lo que origino el área bajo la curva de menor superficie observado en el grafico ROC; esto debido a la obtención de resultados falsos positivos y al reducido número de muestras analizado en el artículo mencionado.
Las gráficas de embudo “Funnel Plot” fueron asimétricas, tanto para sensibilidad como especificidad. Uno de los parametros que evalua este tipo de graficas es el sesgo de publicacion; dentro de las posibles causas de este error sistematico esta la falta de difusion de estudios negativos, poco interesantes, de pequena escala o de baja calidad metodologica, lo que conlleva a encontrar estudios con desenlaces positivos (24).
Una de las razones de haber encontrado estudios positivos puede ser la presencia del sesgo del lenguaje (publicacion de estudios que no tienen hallazgos significativos en otros idiomas diferentes al ingles) lo que hace menos probable que se encuentren dichos estudios "negativos", ya que la mayoría de estudios “positivos” se publican en ingles. Otra posible causa del sesgo de publicacion es la ausencia de estudios con tamanos de muestras no representativos, lo que aumentaria aun mas la apreciacion de positividad de las pruebas evaluadas.
En esta revision se rechazo la hipotesis planteada de que mas del 90% de la bibliografia revisada reportara caracteristicas operativas de sensibilidad y especificidad de la prueba E-test iguales o superiores en un 95%. Aunque el acuerdo entre las dos pruebas en estudio fue muy bueno, solamente el 87% de los estudios lograron cumplir la hipotesis, debido en parte a la falta de estandarización del E-test en antibioticos diferentes a la claritromicina y a la poca utilizacion de estas tecnicas en conjunto (DA y E-test) en particular en laboratorios de rutina.
A manera de conclusion, se puede anotar que la prueba de E-test demostro tener buen acuerdo en sensibilidad y especificidad para detectar susceptibilidad antimicrobiana en aislamientos clinicos de H. pylori, sin embargo no iguala ni supera las caracteristicas operativas del método de referencia. El E-test puede ser utilizado de manera rutinaria para evaluar susceptibilidad de H. pylori a claritromicina y amoxicilina, pero deben realizarse mas estudios para evaluar si esta tecnica puede ser util en la evaluacion de susceptibilidad de H. pylori a levofloxacina.