
Aislamiento e identificación de microorganismos del género Methanococcus y Methanobacterium de cuatro fuentes de Bogotá D.C.
Paola Andrea Acuña González1, Lisvet Sofía ángel García1, Elizabeth Borray Montoya1, Lucia Constanza Corrales2, Ligia Consuelo Sánchez2
1Bacteriólogas y Laboratoristas Clínicas Universidad Colegio Mayor de Cundinamarca
2Msc. Docentes Programa de Bacteriología y Laboratorio Clínico, Facultad Ciencias de la Salud, Universidad Colegio Mayor de Cundinamarca
Correspondencia: lcorralesr@unicolmayor.edu.co
Recibido: 05/06/08 Aceptado: 10/08/08
Los resultados permitieron evidenciar la presencia de bacterias de los géneros Methanococcus y Methanobacterium a partir de las fuentes seleccionadas para el estudio. Se concluyó que el mejor método para la conservación de estos géneros es la congelación con la adición de agentes reductores y glicerol como criopreservante.
Palabras clave: bacterias metanogénicas, anaerobiosis, producción de metano, simbiosis metabólica.
The procedures followed included the sample taking in an anaerobic environment, isolating, in selective recipe and identification of the microscopic characteristics with Gram’s coloration, macroscopic characteristics in the selective media and verification of methane through a sample. The final results allowed evidencing bacteria’s presence such as Methanococcus and Methanobacterium from the sources selected for the study. It was concluded that the best method for the conservation of these species is freezing these samples with the addition of reducing agents and glycerol which acts as a criopreservante.
Key words: methanogenic bacterium, anaerobiosis, methane production, metabolic symbiosis.
Existen varios grupos de bacterias metanogénicas que se diferencian entre si por su morfología; se pueden encontrar bacilos y cocos filamentosos, agrupados en cadenas, diplococos, tetradas y racimos. Pueden desarrollarse a temperaturas que van desde a 38°C a 75°C y su afinidad al Gram es variable (4). Su metabolismo se caracteriza por integrar las vías biosintéticas y bioenergéticas para la producción de ATP. En condiciones de ausencia de hidrógeno, oxidan compuestos para la obtención de electrones (5). Estas bacterias permiten ser empleadas en diferentes procesos biotécnológicos en sistemas anaerobios: como componente de biorreactores para descomposición de basura orgánica (6), para la producción de gas metano a partir de estiércol de cerdo (7); como modelo experimental en simulación de suelos de otros planetas (8), entre otros.
Los sistemas anaerobios desarrollan procesos fermentativos de los cuales se obtienen productos finales estables y una producción celular muy baja, alrededor del 3% de la materia orgánica presente en el agua residual es convertida en masa celular y el 97% restante es convertido por catabolismo en CH4 y CO2 como productos finales estables (9).
Teniendo en cuenta la importancia de estos microorganismos en los procesos de bioremediación para la conservación del medio ambiente, este estudio planteó como objetivo el aislamiento y fenotipificación de dos géneros de bacterias metanogénicas (Methanobacterium y Methanococcus) a partir de cuatro fuentes naturales, utilizando dos medios selectivos (Barker - Taha y Stadtman – Barker) respectivamente, y con el propósito de conservarlas en el cepario de la Universidad Colegio Mayor de Cundinamarca.
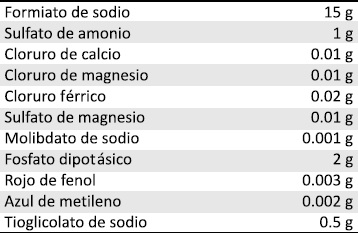
Tabla 1. Reactivos utilizados para la preparación de 1000mL del medio Methanobacterium (Barker-Taha)

Verificación de presencia de microorganismos en las muestras
Se realizaron coloraciones de Gram de las muestras directas de las cuatro fuentes para verificar por microscopía la presencia de bacterias.
Aislamiento y obtención de los microorganismos
Los medios selectivos utilizados para el aislamiento fueron Barker-Taha (MB) para Methanobacterium y
Stadtman–Barker (MC) para Methanococcus (10). Estos medios incluyen diversos sustratos que son utilizados por estos microorganismos como fuente de energía para su crecimiento y metabolismo, Tabla 1 y 2.
La preparación del medio (MB) requiere que una vez se esterilice, se le añaden las siguientes soluciones: carbonato de sodio 0.50 g en 10 mL de agua destilada y sulfuro de sodio 9 (H2O) 0.1g en agua destilada 10 mL.
Pre-reducción de los medios: para los medios líquidos, la pre-reducción se hizo mediante choque térmico, durante 10 minutos a a 100°C en baño maría y luego se enfriaron en chorro de agua fría con el fin de desplazar el O2 que pudiera encontrarse en el tubo. La pre-reducción de los agares se realizó dejando los medios por 2 horas en la jarra de anaerobiosis, utilizando los generadores de atmósfera (AnaeroGen OXOID) (11). A la prueba de esterilidad se le hizo un seguimiento de 72 horas para descartar contaminación con microorganismos aerobios y prueba de selectividad para verificar el desarrollo de bacterias anaerobias, con la inoculación de Clostridium spp. como control.
Tabla 2. Reactivos utilizados para la preparación de 1L de medio Methanococcus (Stadtman-Barker).
Inoculación de la muestra: se inocularon 100μL de cada muestra en los medios líquidos para Methanococcus y Methanobacterium; se realizó coloración de Gram para verificar la presencia de bacterias; los cultivos se incubaron durante 15 días a 37°C en atmósfera de anaerobiosis (AnaeroGen – OXOID). A los 15 días se verificó el crecimiento bacteriano por turbidez en el medio y se realizó la siembra en los medios sólidos MC y MB pre-reducidos; se incubaron durante 15 días a 37°C en condiciones de anaerobiosis y se verificó la presencia de bacilos y cocos en el crecimiento obtenido en los medios líquidos y en los medios sólidos mediante coloración de Gram.
Identificación fenotípica y producción de gas metano
El aislamiento de colonias en los medios sólidos MC y MB confirmaron la presencia de bacterias metanogénicas. La verificación de la producción metabólica de gas metano, se realizó mediante la esterilización previa de cada uno de los elementos que componían el sistema de producción de metano: tubos 16 x 150mm con desprendimiento lateral, tapones de caucho, mangueras en látex de 20 cm. y pinzas en garra. Posteriormente en cabina de flujo laminar se armó el sistema, se envasó el medio de cultivo y se inoculó antes de sellar el sistema.
Los medios de cultivo utilizados fueron MC y MB líquidos en cantidad de 6 mL para proporcionar espacio suficiente para el almacenamiento del gas producido por las bacterias. El inóculo provino de las colonias obtenidas en los medios sólidos MC y MB debido a que la biomasa bacteriana obtenida en ellos fue mayor que en los medios líquidos. La medición cualitativa se hizo por la técnica de desplazamiento de agua contenida en la probeta (12,13), evidenciado por la producción de burbujas generadas por el gas y el aumento del volumen final del agua. El objetivo de utilizar este sistema fue controlar la posible pérdida del gas producido por las bacterias durante la incubación y verificar la presencia del gas metano.
Tabla 3. Resultados Gram directo
Aislamiento y obtención de los microorganismos
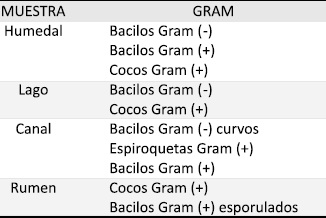
Los datos obtenidos del aislamiento bacteriano en los medios líquidos y sólidos MC y MB indicaron crecimiento de bacterias con características compatibles con Methanococcus y Methanobacterium. La verificación morfológica mediante coloración de Gram se presentan en las Tablas 4 y 5.
Las características macroscópicas de las colonias obtenidas en los agares fueron las siguientes: en el agar MC para Methanococcus se observó la presencia de colonias puntiformes, pequeñas de color amarillo pálido y en el agar MB para Methanobacterium las colonias que crecieron fueron redondas grandes, pegajosas, brillantes, que toman el color del medio (café). En las Figura 1 y 2 se observan las colonias obtenidas en los agares MC y MB.
Tabla 4. Resultado Gram de caldo MC y MB
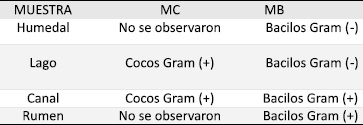
Tabla 5. Resultado Gram de los agares MC y MB.
Figura 1. Colonias obtenidas en el agar MC. (Muestra canal de aguas Av. 127).

Figura 2. Colonias obtenidas en el agar MB. (Muestra aguas de Lago Timiza).
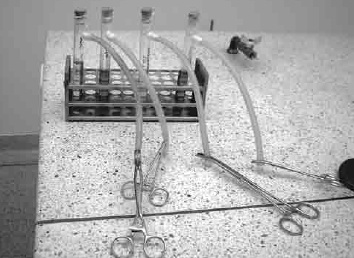
Figura 3. Montaje realizado para la comprobación cualitativa de metano.
Los medios selectivos empleados (Methanococcus Stadtman-Barker y Methanobacterium Barker-Taha) permitieron evaluar el crecimiento de bacterias metanogénicas aunque no se obtuvo crecimiento óptimo a partir de todas las muestras analizadas (14).
Producción de gas metano
La capacidad metabólica de los microorganismos para producir metano se verificó por el aumento del volumen del agua en las probetas, que es directamente proporcional al gas producido por los microorganismos aislados Methanococcus y Methanobacterium, Figura 3 y 4.
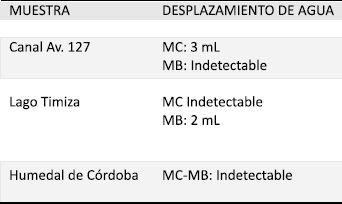
En el montaje que correspondía al medio MC del canal de aguas de la Av. 127 se observó un aumento de 3 mL del volumen de agua; pero no en el medio MB de la misma muestra. Se obtuvo un aumento de 2 mL del volumen de agua en el montaje del medio MB de la muestra de aguas estancadas del Lago Timiza y no el medio MC de la misma muestra. Tampoco hubo aumento del volumen de agua en los montajes realizados para el Humedal de Córdoba de los medios MC y MB, Tabla 6.
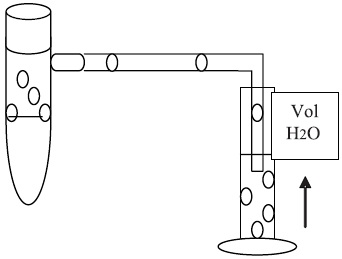
Figura 4. Representación esquemática del desplazamiento de agua por burbujeo.
Tabla 6: Desplazamiento de agua producido a partir de las diferentes muestras inoculadas en MC y MB.
En la muestra del Humedal de Córdoba se vio crecimiento de bacilos Gram positivos en el caldo
MB pero no hubo crecimiento en el caldo MC. Sin embargo, al hacer el aislamiento en medio sólido MC hubo crecimiento escaso de cocos Gram positivos. En el medio sólido MB crecieron bacilos Gram negativos que se habían evidenciado en el caldo. Estos resultados pueden ser explicados por la baja biomasa obtenida en el medio líquido relacionada con la dificultad para la adaptación y el desarrollo de estos microorganismos in vitro.
El crecimiento bacteriano obtenido del rumen en los medios líquidos MC y MB tiene el mismo comportamiento al del Humedal de Córdoba. Sin embargo, al hacer el aislamiento en los medios sólidos, no se logró recuperar ningún microorganismo. Este resultado parece estar relacionado con la calidad de toma de muestra ya que estos microorganismos son sensibles a la presencia de oxígeno, así sea en muy bajas proporciones (0.5–2%) o por tiempos cortos, factor que induce procesos de intoxicación y muerte bacteriana, supuesto que se sustenta en que al tomar la muestra del rumen, la panza del animal sacrificado estaba rota y el tiempo que transcurrió entre esta toma y la introducción de éste en la jeringa fue prolongado. La baja biomasa obtenida a partir de la muestra del rumen en los medios líquidos y la ausencia de crecimiento en los medios sólidos conllevó a descartar esta muestra dentro del estudio.
La morfología obtenida en los Gram de ambos caldos, MC y MB presenta concordancia con la selectividad según el fundamento del medio, además las estructuras observadas son características de las Archaeas Metanogénicas (5). Aunque en los protocolos establecidos por Chantereau (9) para el cultivo de los géneros Methanobacterium y Methanococcus, refiere que el crecimiento se puede obtener después de 7 días a partir de la inoculación en los medios de cultivo, en este trabajo se evidenció que los microorganismos pertenecientes a estos géneros son de crecimiento lento, estableciéndose como tiempo óptimo de desarrollo 15 días.
Las bacterias metanogénicas ofrecen una gran variedad de aplicaciones biotecnológicas si se tiene en cuenta que degradan gran variedad de desechos (solas o en consorcios). También son de interés industrial ya que a partir de materiales de desecho producen gas metano, útil porque genera energía al ser usado como combustible. A partir del estudio se plantean posibilidades de aplicación como en rellenos sanitarios, en los cuales se siembran con otras bacterias para generar este gas, combustible que puede ser utilizado para el propio mantenimiento de las instalaciones del relleno, posibilidad que se puede reproducir en otros sistemas como el de fangos activados para el tratamiento de aguas residuales, entre otros. Teniendo en cuenta su importancia y los resultados obtenidos en esta investigación, se puede anotar que la mejor forma de conservarlas en el cepario de la Universidad Colegio Mayor de Cundinamarca, para posteriores estudios, es por congelación con glicerol dada su vulnerabilidad a los ambientes aeróbicos y a las condiciones in vitro.