
Cariotipo del tití gris (Saguinus leucopus): similitudes con el cariotipo humano
Juan Hember Tabares1, Carlos Humberto Fierro1, Paola Del Pilar Pulido2, Humberto Ossa Reyes3
1Biólogo. Laboratorio de Genética y Biología Molecular Ltda.
2Bióloga. Maestría en Ciencias Biológicas U. Nacional de Colombia
3Biólogo Genetista. Laboratorio de Genética y Biología Molecular Ltda.
Correspondencia: hossa@cable.net.co, crazybiostica@gmail.com
Recibido: 25- 08-09 / 15-09-09
Palabras clave: cariotipo, cromosomas, primates, quimerismo, Saguinus leucopus.
Key Words: chimerism, chromosomes, karyotype, Saguinus leucopus.
Los miembros de la familia Callithrichidae, a la cual pertenece S. leucopus, descienden de especies de mayor talla, que durante un período de varios millones de años han adquirido uñas tipo garra, perdiendo el pulgar oponible en las manos y el tercer molar; además, tienen la característica de presentar partos múltiples, siendo el gemelar el más común (4). Los reportes moleculares de Schneider y su equipo (5) demostraron que Saguinus es el género base de los Callithrichidae; también los estudios citogenéticos han llevado a esta conclusión (6).

Figura 1. Individuo de la especie S. leucopus.
Figura 2. Procedimiento de toma de la muestra.
Nagamachi y Pieczarka presentaron el cariotipo de S. midas niger, estudiado por bandas G, C y NOR (7). En este aspecto, se destaca el estudio de Mendes y de Souza, que establecieron los cariotipos de ocho especies brasileñas de Saguinus (S. fuscicollis fuscicollis, S. fuscicollis weddelli, S. bicolor bicolor, S. bicolor martinsi, S. mystax mystax, S. imperator imperator, S. midas midas y S. midas niger) (8). El objetivo de este estudio fue analizar el cariotipo del tití gris (Saguinus leucopus) y compararlo con el cariotipo humano.
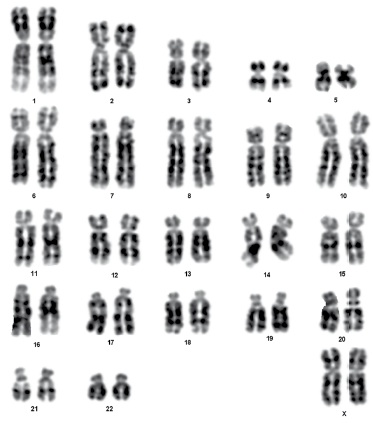
Figura 3. Cariotipo 46, XX de una hembra S. leucopus.
Las imágenes de bandas Q fueron tomadas en microscopio de fluorescencia (Olympus BX50) bajo aumento de 1000X y procesadas en el software KaryoView (Elja Inc.); se invirtieron los tonos de las metafases para facilitar el análisis: las bandas oscuras corresponden a las zonas más fluorescentes. Las imágenes de bandas G se tomaron en microscopio de luz blanca (Olympus BX50) a un aumento de 1000X y se procesaron sin ninguna novedad en el software KaryoView (Elja Inc.). En total se capturaron y analizaron 50 metafases de la hembra y 50 del macho.
A partir de las metafases obtenidas se elaboró un ideograma para el cariotipo de S. leucopus. El orden de los cromosomas en el cariotipo se asignó teniendo como referencia el trabajo de las investigadoras brasileñas Mendes y de Souza (8). Se comparó el cariotipo del tití gris con el humano. Los cariotipos humanos utilizados en la comparación pertenecen a individuos normales.
Métodos moleculares. El ADN de S. leucopus al igual que el de H. sapiens fue aislado mediante el kit Wizard (Promega) y posteriormente amplificado para una región de 345 pb del gen de la protrombina humana (Factor II) y una región de 203 pb del gen Metilentetrahidrofolato Reductasa (MTHFR) (12). Posteriormente, se procedió a realizar digestión enzimática con Mnl I y Hinf I, respectivamente, para determinar la presencia de las mutaciones G20210A para el Factor II y C677T para el MTHFR, las cuales se asocian en humanos a enfermedad vascular y ateroesclerosis (13). La electroforesis de los productos de digestión se realizó en gel de agarosa al 2% y su visualización fue y con bromuro de etidio. El ADN humano pertenece a controles sanos, libres de las mutaciones.
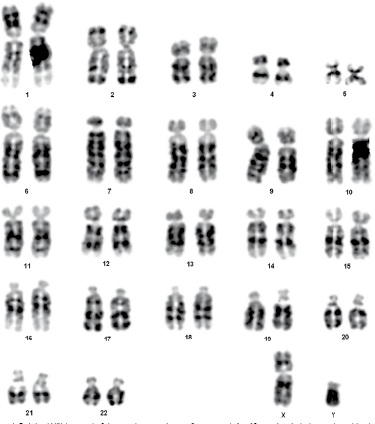
Figura 4. Cariotipo 46,XY de un macho S. leucopus. Las zonas altamente fluorescentes de 1q y 10q son el resultado de una sobreposición de estos cromosomas en la metafase, no representan bandas de los cromosomas.
Se observó similitud completa entre los cromosomas X de ambas especies, Figura 6, A,B,C; asimismo, entre el cromosoma 5 de S. leucopus y el 19 del ser humano, Figura 6, D- F. El brazo corto del cromosoma 7 humano presenta similitud con 2p de S. leucopus; 7q de H. sapiens tiene correspondencia con 12q del tamarino, Figura 7, A-E. Los satélites de los cromosomas acrocéntricos del tití gris presentan una configuración distinta a la de los cromosomas acrocéntricos humanos, Figura 7, F y G.
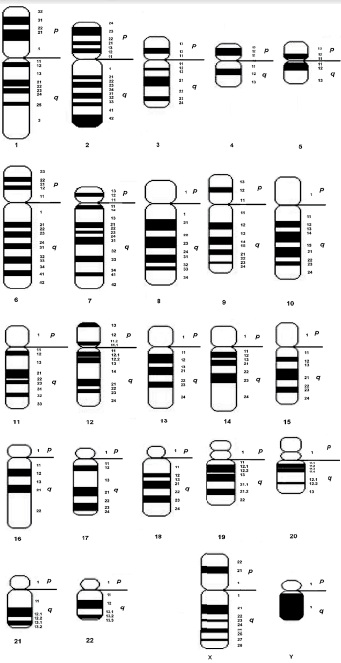
Figura 5. Ideograma del cariotipo de S. leucopus, resolución 300-400 bandas.
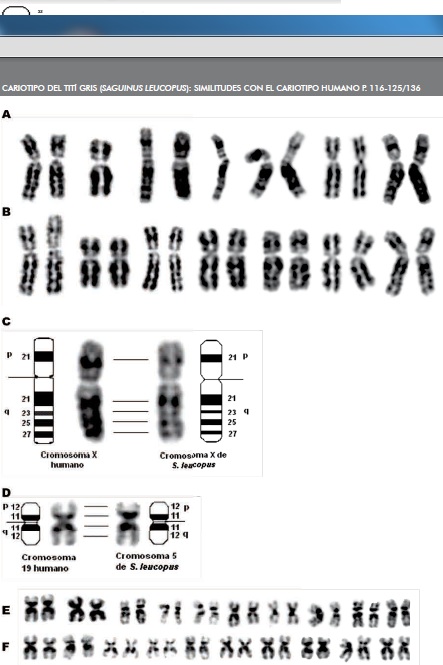
Figura 6. A. Cromosomas X de diferentes personas. B. Cromosomas X de S. leucopus. C. Comparación del bandeamiento entre cromosomas X de las dos especies. D. Comparación del bandeamiento entre cromosomas 19 de H. sapiens y 5 de S. leucopus. E. Cromosomas 19 de diferentes personas. F. Cromosomas 5 de S. leucopus.
El cromosoma 1 en ambas especies presenta gran similitud. Si el cromosoma 1 de S. leucopus es rotado 180°, se observa que todo el brazo q se asemeja a 1p humano, con una posible inversión que involucra la región central del brazo, Figura 8, A-C. No obstante, la gran región heterocromática de 1q12 humano parece estar ausente en 1p de S. leucopus. No se puede afirmar con certeza la presencia de la banda oscura 1q31 distintiva del cariotipo humano en 1p de S. leucopus siendo difícil la determinación citogenética del origen del brazo corto del cromosoma 1 del tití gris.
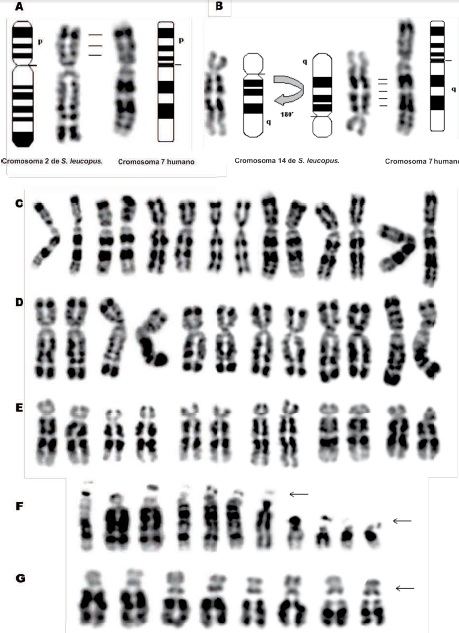
Figura 7. A. Comparación del bandeamiento entre el brazo corto del cromosoma 2 de S. leucopus y el brazo corto del cromosoma 7 de H. sapiens. B. Comparación del bandeamiento entre el brazo largo del cromosoma 14 de S. leucopus y el brazo largo del cromosoma 7 de H. sapiens. C. Cromosomas 7 de diferentes personas. D. Cromosomas 2 de S. leucopus. E. Cromosomas 14 de S. leucopus. F. Cromosomas acrocéntricos humanos. G. Cromosomas acrocéntricos de S. leucopus. Obsérvese la particular configuración doble de satélites en S. leucopus, que no se observa en seres humanos.
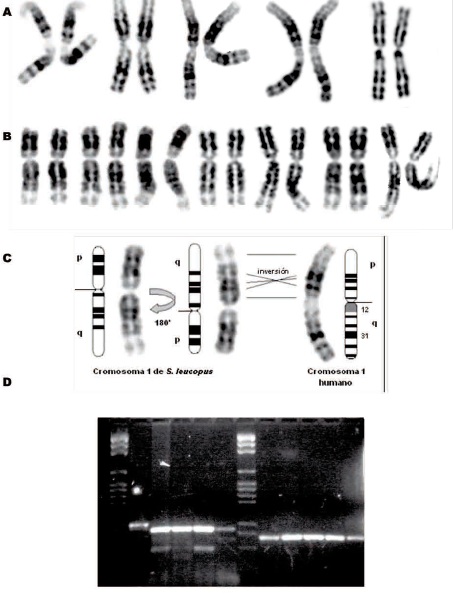
Figura 8. A. Cromosomas 1 de diferentes personas. B. Cromosomas 1 de S. leucopus. C. Comparación del bandeamiento entre cromosomas 1 de las dos especies. D. Gel del estudio molecular, carriles 1-6 Factor II, carriles 7-12 MTHFR. Carril 1: escalera Pgem; carril 2: S. leucopus hembra (sin Digestión); carril 3: S. leucopus hembra; carril 4: S. leucopus macho; carril 5: H. sapiens N°1; carril 6: H. sapiens N°2. Carril 7: escalera Pgem; carril 8: S. leucopus macho (sin Digestión) 9. S. leucopus hembra; carril10: S. leucopus macho; carril 11: H. sapiens N°1; carril 12: H. sapiens N°2.
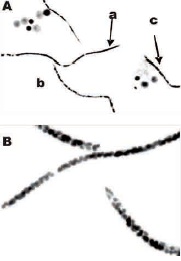
Figura 9. A. a. Microfilaria, b. Núcleos, c. Metafase. Aumento 400X. B. Microfilaria, aumento 1000X
Los procedimientos moleculares dieron lugar a la banda de amplificación de 345 pb para el Factor II y
203 pb para el MTHFR tanto en S. leucopus como en H. sapiens, siendo evidente la similitud (al menos en el tamaño de la región amplificada de los dos genes) entre las dos especies. Los individuos estudiados tanto de S. leucopus como de H. sapiens no presentaron las mutaciones G20210A para el FII y C677T para el MTHFR, Figura 8D.
Se observó que la pareja de tamarinos presentaban infección por un parásito cuya morfología encaja con
microfilaria, una fase larval de nemátodos parásitos que se encuentran en la corriente sanguínea. Fox y colaboradores (14) durante un estudio de la bioquímica hematológica de S. leucopus cautivos, encontraron que 22 de sus 29 individuos tenían microfilaremia, condición que se vio en los animales de la presente investigación, Figura 9.
Según Murphy y su equipo el cromosoma 1 humano parece haberse conservado muy bien respecto al cromosoma ancestral del que se originó en el antepasado de todos los mamíferos placentarios (15). El brazo q del cromosoma 1 alberga dos grupos importantes de hotspots para rupturas, lo que hace difícil encontrarlo intacto en muchas especies; creemos que S. leucopus es una de ellas. Por otra parte, para explicar el cariotipo quimérico del tití gris macho estudiado, nos remitimos a lo observado en seres humanos, donde el quimerismo congénito se da gracias a la persistencia de transfusión de células madre hematopoyéticas durante el desarrollo fetal, que puede permanente o durar por muchos años (16,17).
En consecuencia, el quimerismo observado en el tamarino macho se puede explicar por una transfusió materno fetal o feto fetal en el útero materno, siendo probable en esta especie de primates donde los embarazos múltiples son frecuentes. En el trabajo de Mendes y de Souza (8) se reportó quimerismo 46,XX/46,XY en todas las especies de Saguinus analizadas.
Para nuestro conocimiento, esta es la primera descripción del cariotipo de S. leucopus, en la que adicionalmente se ha hecho un análisis objetivo de los posibles cromosomas y bandas que no se han visto modificadas durante la evolución en ambas especies. Esto arroja resultados interesantes, que nos conducen a afirmar que si se emplean sondas fluorescentes para genes humanos de los cromosomas 1p, 7, 19, y X, estamos en capacidad de predecir el sitio blanco al cual hibridarán en el cariotipo de S. leucopus, y por lo tanto, la ubicación de los genes en el genoma del tamarino.
Los resultados de este estudio ayudarán a la potencial identificación del origen geográfico de los S. leucopus que han llegado a los centros de rescate para su reincorporación al hábitat natural de los animales que aprueben los procesos de rehabilitación médico biológica. Para esto es necesario contrastar los resultados obtenidos en esta investigación con los análisis genético poblacionales propuestos por otros investigadores (3), así como integrar estos resultados en dichos análisis. La identificación de grupos poblacionales y su distribución facilitará la asignación de territorios nacionales para generar áreas de conservación específicas para el tití gris.