Bacterias anaerobias presentes en surco gingival de pacientes con prótesis parcial fija
Liliana Sánchez Lerma1, Diana Milena Estupiñán Torres2, Geovana Katherine Reyes Guevara3, José Alberto Acosta Rueda4.
1Magister en Microbiología Médica, Docente Facultad de Medicina, Universidad Cooperativa de Colombia, Villavicencio.
2Especialista en Odontología Legal y Forense. Docente Facultad de Odontología, Universidad Cooperativa de Colombia, Villavicencio.
3Periodoncista. Docente Facultad de Odontología, Universidad Cooperativa de Colombia, Villavicencio.
4Ortodoncista, Decano Facultad de Odontología Universidad Cooperativa de Colombia, Villavicencio. Correspondencia: liliana1823@hotmail.com
Recibido 23-04-08 / Aceptado 15-05-08
Las muestras obtenidas con punta de papel, fueron aisladas en agar sangre e incubadas en medio anaerobio. Se les realizó la prueba de aerotolerancia y la identificación se hizo con el sistema RapID TM ANA II System Remel. Se aislaron 12 bacterias anaerobias correspondientes a: 8,33% bacilos Gram negativos; 58,33 % bacilos Gram positivos y 33,33 % cocos Gram positivos. En el grupo control ninguna bacteria anaerobia fue aislada. únicamente fueron observados cocos facultativos Gram positivos. Aunque no se ha descrito que la presencia de placa en prótesis fijas tenga alguna clase de impacto negativo sobre los tejidos periodontales, la acumulación de ésta por un período extendido puede convertirse en un factor de riesgo para un problema de salud pública, como la enfermedad periodontal. Los resultados de este estudio confirmaron que la presencia de prótesis fijas resultó en un cambio en la composición de la microflora anaeróbica del surco gingival, compatible con enfermedad periodontal.
Palabras clave: bacterias anaerobias, enfermedad periodontal, prótesis fija, salud pública, surco gingival.
Present anaerobic bacteria in gingival sulcus of patients with fixed partial dentures Recently, the biological aspects of fixed reconstructions have been given attention because dental materials have great capacity to accumulate and retain plaque. The microflora at both tooth and fixed partial prostheses can be identified as biofilms, which are composed of microcolonies of bacterial cells distributed in a shaped matrix. The purpose of this study was to isolate anaerobic bacteria in gingival sulcus from patients during fixed partial denture treatment. 45 samples were analyzed. 30 patients with fixed partial dentures treatment and 15 subjects without partial denture treatment were enrolled in the study. Microbiologic samples were obtained by inserting paper points into the gingival sulcus.
Samples were cultured for anaerobic bacteria on blood agar. The plates were placed into an anaerobic chamber. Later, aerotolerance tests were performed for each different colony. RapID TM ANA II System Remel was used for identification of anaerobes. A total of 12 anaerobic bacteria were observed: 8.33 % gram–negative bacilli, 58.33 % gram-positive bacilli, 0 % Gram-negative cocci, and 33.33 % gram-positive cocci. In the control group none anaerobic bacteria was isolated. Only facultative gram-positive cocci were observed (100%). The results of this study have confirmed that the presence of fixed partial dentures resulted in a change in the composition of the anaerobic microflora of the gingival sulcus, compatible with periodontal disease.
Key Words: anaerobial bacteria, fixed partial dentures, gingival sulcus, periodontal disease, public health.
Está demostrado que existen asociaciones especificas entre la bacteria y la biopelícula dental (3-5). Adicionalmente, las superficies rugosas permiten la acumulación de placa lo que facilita el desarrollo de la gingivitis, que es la forma más leve de enfermedad periodontal, siendo una de las entidades más comunes a nivel mundial y una de las principales causas de pérdida dentaria (1).
El surco gingival es reconocido como el nicho anaeróbico más completo que existe en el organismo, debido a que es un sitio muy pobre en oxígeno. En condiciones normales habitan en este surco gran cantidad de bacterias en donde predominan los cocos Gram positivos, bacilos Gram positivos y Gram negativos. Esta población microbiana, más ó menos constante en cantidad, es la que se conoce como microbiota del surco gingival, pero cuando se supera la población bacteriana, y especialmente cuando este surco ha sido invadido por bacterias relativamente patógenas o hay ruptura del equilibrio defensa/bacteria, se establece una patología gingival que puede evolucionar hacia el periodonto.
La periodontitis, que antes se consideraba una enfermedad limitada a las encías, ocasiona una respuesta inflamatoria sistémica con elevación de varios reactantes de fase aguda como la proteína C reactiva y el fibrinógeno (6,7). La elucidación de los cambios microbianos durante procedimientos prostodonticos fijos puede proveer información acerca de la respuesta gingival vista durante esta clase de procedimiento. En la gingivitis una gran cantidad de placa dental y cambios cualitativos en cuanto a la composición bacteriana en placa supra y sub-gingival se encuentra en contraste con una gingiva saludable (8).
La inserción de prótesis fija puede tener un impacto negativo en los tejidos periodontales. Varias observaciones clínicas han reportado la formación de bolsas y recesión gingival que puede ser más prevalente alrededor del diente tratado prostodonticamente (1,9). En particular, el desplazamiento del margen subgingival está asociado con un efecto negativo sobre el periodonto y es una de las mayores razones por la cual ocurren fallas en las coronas y en las prótesis parciales fijas (10). El objetivo de este estudio fue determinar las bacterias anaerobias presentes en el surco gingival de pacientes durante tratamiento prostodontico fijo.
El grupo experimental se conformó de treinta pacientes con tratamiento prostodontico fijo. El rango de edad de los pacientes fue entre 20 a 45 años (promedio de edad 32.5 años). La selección se hizo de acuerdo a los siguientes criterios: i. La prótesis no debía usarse junto con una prótesis removible, ii. La prótesis debía tener un tiempo mínimo de seis semanas; iii. Las prótesis debían estar bien adaptadas; iv. Si los pacientes tenían más de una corona fija, únicamente se elegía una corona al azar para permitir independencia en la observación. Los criterios de exclusión fueron: pacientes que por estado de salud no estaban en condiciones de ser llamados para el estudio, abuso de alcohol, abuso de drogas, desordenes psiquiátricos y alguna enfermedad sistémica.
El grupo control estuvo formado por quince sujetos sin tratamiento prostodontico. El rango de edad de los pacientes fue entre 20 a 45 años (promedio de edad 32.5 años). Se tuvieron en cuenta los criterios de exclusión antes mencionados.
Procedimiento clínico: se tomaron datos relevantes para la historia clínica (no analizados aquí) antes de la toma de la muestra. La placa supra-gingival fue removida con una cureta estéril y luego descartada. Los sitios de donde se obtuvo la muestra fueron aislados con algodón y cada sitio fue secado con aire seco. Las muestras microbiológicas sub-gingivales se obtuvieron insertando puntas de papel de uso endodóntico de 30 mm de diámetro durante 15 segundos dentro del surco gingival del pilar de la prótesis fija de los pacientes del grupo experimental y de un diente seleccionado al azar de los pacientes del grupo control.
Procesamiento microbiológico: las muestras microbiológicas obtenidas de todos los pacientes se colocaron en caldo Tioglicolato y llevadas inmediatamente al laboratorio de microbiología para el procedimiento de cultivo anaerobio. Las muestras fueron sembradas en agar sangre y colocadas dentro de campana de anaerobiosis que contenía una mezcla de gas de 80% a 90% de nitrógeno, 5% a 10% de hidrógeno y 5% a 10% de CO2 e incubadas a 37ºC por 48 a 72 horas.
Luego se realizó la prueba de aerotolerancia para cada colonia diferente observada y después se llevó a cabo la coloración de Gram para determinar pureza y morfología. RapID TM ANA II System. Remel, fue usado para la identificación de los anaerobios. La categoría de patogenicidad de la bacteria fue dada de acuerdo a sí el organismo ha sido asociado con enfermedad periodontal progresiva (bacteria sospechosa periodontalmente) o no (bacteria no sospechosa periodontalmente).
Análisis estadístico: para analizar los datos y resultados se utilizó el programa EpiInfo (V.6.04; 2002, CDC, Atlanta GA, USA). Se empleó la prueba de Chi cuadrado para analizar las diferencias encontradas entre los grupos.
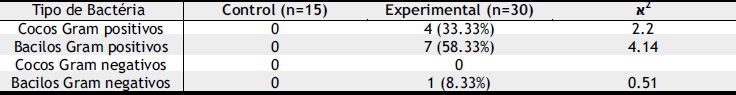
Las prótesis tenían un tiempo de cementación de 6 meses a 2 años. En la Tabla 1 se describe la composición de la microflora encontrada en los grupos experimental y de control con respecto a la morfología y coloración de Gram. Un total de 12 bacterias anaeróbicas fueron observadas: 8.33% bacilos Gram negativos, 58.33 % bacilos Gram positivos y 33.33 % cocos Gram positivos. En el grupo control ninguna bacteria anaeróbica fue aislada. únicamente fueron observados cocos facultativos Gram positivos (100%). En el grupo experimental, un total de 12 bacterias anaeróbicas fueron observadas: 33.33 % cocos y 66.66 % bacilos. Se encontró una diferencia significativa entre la proporción de cocos y bacilos (p= < 0.05).
En la Tabla 2 se presenta la relación de la microbiota anaerobia aislada presente en el surco gingival de pacientes con prótesis parcial fija.
Tabla 1. Distribución de aislados anaeróbicos en los grupos control y experimental para coloración de Gram y propiedades morfológicas.

Chi cuadrado. La diferencia entre ambos grupos es significativa (p= < 0.05).
Tabla 2. Tipos de bacterias aisladas en el surco gingival del grupo experimental.
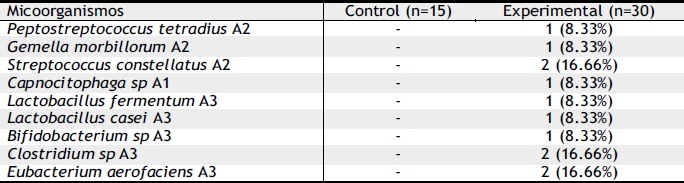
A1= Bacilos Gram negativos; A2= cocos Gram positivos; A3= Bacilos Gram positivos.
Los resultados indican que los dientes con prótesis parcial fija tienen más probabilidad de colonización por bacterias anaeróbicas que los que no presentan esa clase de tratamiento. El análisis de regresión linear mostró una diferencia estadística significativa con un valor p= < 0.05 entre los dientes naturales y las prótesis fijas.
Parkinson y colaboradores indicaron que los ponticos y los pilares con sus cubiertas juegan un papel dinámico, como un componente de la prótesis; el pontico no debe ser considerado como un inserto inerte (porcelana/no precioso) (11). El pontico insertado altera el balance ecológico y puede contribuir al daño de la salud biológica del tejido (1,12). La composición de la flora encontrada es compatible con gingivitis. En este estudio se demostró que durante el procedimiento de prostodoncia fija ocurre un cambio de la microflora marginal asociada a la salud subgingival, que son debidos, principalmente, al desbridamiento marginal y subgingival y al desplazamiento que sufre la gingiva durante la preparación del diente (13-15).
Gemella morbillorum, Bifidobacterium y Capnocitophaga son bacterias involucradas en la enfermedad periodontal yfueron aisladas en este estudio, Jolivet-Gougeun y su grupo(16) reportaron que Capnocitophaga está involucradaen enfermedad periodontal complicada por septicemiacon diseminación a gran variedad de sitios; Kuriyama ycolaboradores (17) indicaron que en su estudio aislaronStreptococcus constellatus a partir de todos los tiposde infección oral. Eubacterium y Peptostreptococcusfueron recuperados únicamente a partir de infeccionesdentoalveolares, mientras que Gemella morbillorum seencontró con más frecuencia en periodontitis que enotras infecciones.
Las prótesis parciales fijas pueden crear un medioambiente donde los microorganismos periodontopatogenos pueden sobrevivir y multiplicarse (18), esto teniendo en cuenta que no hay prótesis que se adapten al diente con un margen perfecto, por lo que siempre se acumula placa, la imprecisión puede ir de 25 a 500 micras. Los resultados del presente estudio, son similares a los obtenidos por Flores-de-Jacoby y colaboradores, quienes concluyeron que la composición de la placa subgingival que rodea la corona y el margen gingival esta alterada (19).
De otro lado, Hojo y su grupo (20) detectaron Lactobacillus fermentum en saliva, pero específicamente no fue asociado con salud periodontal. En contraste Bifidobacterium puede estar asociado dependiendo de la salud periodontal y de la edad del paciente. Van Houte y su grupo (21) mostraron que Lactobacilli tienen una baja afinidad por la superficie de los dientes, lo que sugiere que su asociación con prótesis fijas puede deberse a la retención mecánica que ofrece condiciones de crecimiento.
En nuestro estudio (16.66%) de Lactobacilli fueron aislados.
En el presente estudio fueron aislados Eubacterium aerofaciens en (16.66%), Downes y colaboradores (22)aislaron esta bacteria de bolsas periodontales y abscesosdentoalveolares, Prevotella intermedia, Porphyromonas gingivalis y Fusobacterium nucleatum, los periodontopatógenossospechosos por excelencia no fueron aisladosde ninguna de las muestras de este estudio.
Los presentes hallazgos indican que los patógenos periodontales oportunistas pueden estar presentes en el surco gingival y que sus proporciones pueden incrementarse por alteración de sus condiciones ecológicas. Aunque no se ha descrito que la presencia de placa en prótesis fijas tenga alguna clase de impacto negativo sobre los tejidos periodontales de los dientes pilares adyacentes, la acumulación de placa por un periodo extendido en estos dientes pilares pueden convertirse en un gran factor de riesgo para un problema de salud pública, como lo es la enfermedad periodontal, que es la segunda causa de perdida dental y que conlleva a alteraciones en la masticación, la fonación, la estética y a nivel psicológico, además de su relación con múltiples enfermedades sistémicas (23-25). En conclusión, los resultados de este estudio confirmaron que la presencia de prótesis fijas resultó en un cambio en la composición de la microflora anaeróbica del surco gingival, compatible con enfermedad periodontal.
2. Lee K, Maiden M, Tanner A, Weber H. Microbiota of successful osseointegrated dental implants. J Periodontol 1999;70:131-138.
3. Gerber J, Wenaweser D, Heitz L, Lang N, Persson R. Comparison of bacterial plaque samples from titanium implant and tooth surfaces by different methods. Clin Oral Impl Res 2006;17: 1-7.
4. Socransky S, Haffajee A. Dental biofilms: difficult therapeutic targets. Periodontol. 2002;28: 12-55.
5. Marsh P. Are dental diseases examples of ecological catastrophes? Microbiol. 2003;149:279-294.
6. Ramírez J, Contreras A. ¿Se debe considerar la enfermedad periodontal como un problema de salud publica en Colombia? Colomb Med. 2007; 38:181-182.
7. Marsh P. Dental plaque as a microbial biofilm. Caries Res 2004; 38:204-211.
8. Hall-Stoodley L, Costerton J, Stoodley P. Bacterial biofilms: from the natural environment to infectious diseases. Nat Rev Microbiol. 2004;2:95-108.
9. Van Winkelhoff A, Loos B, Vander Reidjen W, Vander Veiden U. Porphyromonas gingivalis and other putative pathogens in subjects with and without periodontal destruction. J Periodontol 2002;29:1023-1028.
10. Silness J. Fixed Prosthodontics and periodontal health. Dent Clin North Am 1980;24:317-329.
11. Parkinson C, Schaberg T. Pontic design of posterior fixed partial prostheses: Is it a microbial misadventure?. The Journal of Prosthet Dent 1984;51:51-54.
12. Beighton D. The Complex oral microflora of high-risk individuals and groups and its role in the caries process. Community Dent Oral Epidemiol. 2005;33:248-257.
13. Flemming T, Sorensen J, Newman M, Nachnani S. Gingival enhancement in fixed prosthodontics. Part ll: Microbiologic findings. J Prosthet Dent 1991;65:365-72.
14. Leonhardt A, Renvert S, Dahlen G. Microbial findings at failing implants. Clin. Oral Impl. Res 1999;10:339-345.
15. Marsh P. Plaque as a biofilm: pharmacological principles of drug delivery and action in the sub-and supragingival environment. Oral Dis. 2003;9 Suppl1:16-22.
16. Jolivet-Gougeon A, Sixous J, Tamanai-Shacoori Z, Bonnaure- Mallet M. Antimicrobial treatment of Capnocitophaga infections. Int J Antimicrob Agents 2007;29:367-373.
17. Kuriyama T, Karasawa T, Nakagawa K, Yamamoto E, Nakamura S. Bacteriology and antimicrobial susceptibility of gram-positive cocci isolated from pus specimens of orofacial odontogenic infections. Oral Microbiol Immunol 2002;17: 132-135.
18. Van Winkelhoff A, Goene R, Benschop C, Folmer T. Early colonization of dental implants by putative periodontal pathogens in partially edentulous patients. Clinical Oral Implants Res. 2000;11: 511-520.
19. Flores-de-Jacoby L, Zafiropoulos GG, Ciancio S. The effect of crown margins location on plaque and periodontal health. Int J Periodontics Restorative Dent 1989;9:197-205.
20. Hojo K, Mizoguchi Ch, Taketomo N, Ohshima T, Gomi K, Arai T, Maeda N. Distribution of salivary Lactobacillus and Bifidobacterium species in periodontal health and disease. Biosci Biotechnol Biochem. 2007;71:152-157.
21. Van Houte J, Gibbons R, Pulkkinen A. Ecology of human oral Lactobacilli. Infect Immun 1972;6:723-729.
22. Downes J, Olsvik B, Hiom SJ, Spratt DA, Cheeseman SL, Olsen I, Weightman AJ, Wade WG. Bulleidia extructa gen.nov. sp.nov., isolated from the oral cavity. Int J Syst Evol Microbiol. 2000;50:979-983.
23. Wang J-C, Lai C-H, Listgarten MA. Porphyromonas gingivalis, Prevotella intermedia and Bacteroides forsythus in plaque subjacent to bridge pontics. J Clin Periodontol. 1998;25:330-333.
24. Haffajee A, Socransky S. Microbial etiological agents of destructive periodontal diseases. Periodontol. 2000 1994;5:78-111.
25. Vandenbrouke-Grauls C, Savelkoul, P. Periodontal pathogens: a quantitative comparison of anaerobic culture and real-time PCR. FEMS Immunol Med Microbiol. 2005;45:191-199.